Heksogen
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||
| Wzór sumaryczny |
C3H6N6O6 |
||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory |
C3H6N3(NO2)3 |
||||||||||||||||||||||||
| Masa molowa |
222,12 g/mol |
||||||||||||||||||||||||
| Wygląd |
biały, drobnokrystaliczny proszek |
||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||
Heksogen (cyklonit, T4, Hx, RDX – od ang. royal demolition explosive lub research department explosive) – organiczny związek chemiczny, jedna z nitroamin heterocyklicznych, stosowana jako materiał wybuchowy.
Właściwości
Prędkość detonacji cyklonitu wynosi 8440 m/s przy gęstości 1,70 g/cm³. W temperaturze pokojowej jest bardzo stabilny – spala się, nie wybuchając. Do detonacji niezbędne jest użycie zapalnika. Heksogen staje się jednak bardzo wrażliwy w postaci krystalicznej poniżej −4 °C.
Zastosowanie
Heksogen jest jednym z najpotężniejszych materiałów wybuchowych kruszących. Ma dużą siłę kruszącą, jest stabilny podczas przechowywania i bezpieczny dzięki małej wrażliwości na bodźce mechaniczne. Ma szerokie zastosowanie jako militarny materiał wybuchowy, zarówno samodzielnie w postaci różnych ładunków, jak i jako składnik wielu mieszanin. Po dodaniu do niego plastyfikatorów i innych składników powstają plastyczne materiały wybuchowe, takie jak C4, lecz np. Semtex zawiera zamiast niego pentryt. Heksogen jest też składnikiem m.in. A-IX-2, HBX, torpeksu, H-6, heksalu, HTA. Stosowany do napełniania spłonek pobudzających, lontów detonujących i artyleryjskich pocisków małokalibrowych oraz w mieszaninie z trotylem, do napełniania korpusów pocisków artyleryjskich, bomb lotniczych, min i torped.
Historia
Heksogen otrzymano po raz pierwszy w II połowie lat 90. XIX w. Jego szerokie stosowanie rozpoczęło się po opanowaniu bezpiecznych i skutecznych metod syntezy. W czasach II wojny światowej był wykorzystywany w dużych ilościach przez obie walczące strony. Współcześnie jest najważniejszym materiałem wybuchowym o zastosowaniu militarnym.
Otrzymywanie
Heksogen otrzymywany jest w reakcji stężonego kwasu azotowego z urotropiną. Uproszczony zapis reakcji:
- (CH2)6N4 + 10HNO3 → (CH2-N-NO2)3 + 3CH2(ONO2)2 + NH4NO3 + 3H2O
Produktami ubocznymi procesu są azotan amonu i diazotan metanodiolu, CH2(ONO2)2. Związki te powstają także w głównej reakcji ubocznej:
- (CH2)6N4 + 16HNO3 → 6CH2(ONO2)2 + 4NH4NO3
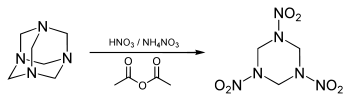
Inną metodą syntezy heksogenu jest nitrowanie urotropiny mieszaniną kwasu azotowego i azotanu amonu w obecności bezwodnika octowego (podobnie produkuje się jeszcze silniejszy oktogen).