- Zespół Aicardiego-Goutièresa
- Prezentacja antygenu
- Barebacking
- Bug chasing
- Kryptokokoza
- Wirus GB-C
- Ludzki wirus niedoboru odporności
- Proteaza HIV-1
- Zespół lipodystrofii HIV
- Zespół nabytego niedoboru odporności
- Poufność
- Mięsak Kaposiego
- Zakażenia okresu noworodkowego
- Bezpieczny seks
- Ostra choroba retrowirusowa
- The Freddie Mercury Tribute Concert
- Mit oczyszczającej mocy dziewicy
- Okienko serologiczne
Zespół nabytego niedoboru odporności
| Syndroma immunitatis defectus acquisiti | |
 Czerwona kokardka jest symbolem solidarności z osobami zakażonymi HIV i chorymi na AIDS | |
| Klasyfikacje | |
| ICD-10 |
B20 |
|---|---|
| ICD-10 |
B21 |
| ICD-10 |
B22 |
| ICD-10 |
B23 |
| ICD-10 |
B24 |
{{Choroba infobox}}
|

| |
| Czynnik chorobotwórczy | |
| Nazwa | |
|---|---|
| Rezerwuar |
człowiek |
| Epidemiologia | |
| Droga szerzenia |
krew, kontakty seksualne, niesterylny sprzęt medyczny, zakażenie przez matkę płodu lub karmionego piersią noworodka |
| Występowanie |
cały świat |
| Prawo | |
| Przymusowe leczenie |
nie |
| Podlega zgłoszeniu WHO |
nie |
Zespół nabytego niedoboru odporności, zespół nabytego upośledzenia odporności, AIDS (od ang. acquired immunodeficiency syndrome lub acquired immune deficiency syndrome), SIDA (od łac. syndroma immunitatis defectus acquisiti) – choroba wywoływana przez ludzki wirus niedoboru odporności (HIV), prowadząca do postępującego upośledzenia odporności osoby zakażonej i ostatecznie do rozwoju zespołu nabytego niedoboru odporności.
Zakażenie ludzkim wirusem niedoboru odporności następuje przez kontakt seksualny, ekspozycję na wydzieliny lub tkanki zawierające wirusa oraz na drodze okołoporodowej. U części chorych w ostrej fazie infekcji pojawia się niecharakterystyczna choroba grypopodobna zwana ostrą chorobą retrowirusową, jednak u większości, mimo replikacji wirusa, spadku limfocytów CD4+ i postępującego upośledzenia funkcji układu immunologicznego, AIDS przez pewien okres przebiega bezobjawowo. Faza objawowa, której wyrazem są rozwijające się zakażenia oportunistyczne i nowotwory, jest następstwem znacznego obniżenia odporności. Ostatecznie dochodzi do rozwoju zespołów chorobowych spełniających kliniczne kryteria rozpoznania zespołu nabytego niedoboru odporności. AIDS jest rozpoznawany również przy spadku liczby limfocytów CD4+ poniżej 200 komórek na mikrolitr.
Diagnostyka zakażenia HIV jest oparta o badania serologiczne wykrywające przeciwciała powstałe w odpowiedzi immunologicznej skierowanej przeciw HIV, które są wykrywane metodą immunoenzymatyczną, ale do ostatecznego rozpoznania konieczne jest wykonanie badania potwierdzającego zakażenie, w którym wykorzystuje się metodę western blot. W leczeniu zakażenia HIV stosuje się wielolekową terapię antyretrowirusową, polegającą na jednoczesnym zastosowaniu kilku leków antyretrowirusowych.
Historia
W 1981 amerykańskie Centra Kontroli Chorób (CDC) opublikowały w swoim czasopiśmie opis 5 przypadków rzadkiego oportunistycznego zapalenia płuc wywołanego przez Pneumocystis carinii u młodych homoseksualnych mężczyzn oraz zachorowań na rzadki nowotwór – mięsak Kaposiego. Już do końca 1981 rozpoznano ponad 335 przypadków AIDS, z czego 158 chorych zmarło. Początkowo chorobę rozpoznawano u homoseksualnych mężczyzn i u osób przyjmujących dożylnie narkotyki, a także chorych na hemofilię, którzy musieli często przyjmować preparaty krwiopochodne. Na przełomie 1982 i 1983 opisano przypadki choroby u kobiet na skutek kontaktów heteroseksualnych z mężczyznami chorymi na AIDS, a także chorobę u niemowląt chorych matek, co potwierdziło możliwość zakażenia drogą heteroseksualną i okołoporodową. W 1982 chorobę wcześniej nazywaną gay related immunodeficiency (GRID) nazwano acquired immunodeficiency syndrome (AIDS). Jeszcze przed rozpoznaniem czynnika etiologicznego, ustalono, że choroba ma podłoże zakaźne i przenosi się drogą krwiopochodną i wydano pierwsze zalecenia dotyczące zapobiegania chorobie. W 1983 Luc Montagnier i współpracownicy z Instytutu Pasteura opisali wyizolowany od chorego na AIDS z limfadenopatią retrowirus, który został później nazwany lymphadenopathy associated virus (LAV). Niezależnie od Luc Montagniera, grupa Roberta Gallo z Narodowych Instytutów Zdrowia wykazała obecność u chorych na AIDS retrowirusa podobnego do HTLV. Gallo nazwał go HTLV-III. W 1985 opracowano komercyjne testy w kierunku HIV. W 1986 ujednolicono nomenklaturę i wirus wywołujący AIDS został nazwany human immunodeficiency virus (HIV). W 1987 opracowano pierwszy lek antyretrowirusowy – zydowudynę. Dalszy postęp w odkrywaniu kolejnych leków pozwolił na opracowanie w 1996 wysoce aktywnej terapii antyretrowirusowej (HAART), składającej się z połączenia kilku skutecznych leków antyretrowirusowych.
Epidemiologia
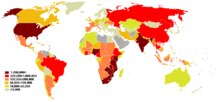
Według szacunkowych danych Światowej Organizacji Zdrowia (WHO) w 2015 na świecie żyło 36,7 milionów ludzi zakażonych HIV, z czego 3,2 miliona stanowiły dzieci poniżej 15 roku życia. Ocenia się, że zakażenie HIV od początku epidemii dotknęło 78 milionów osób, z czego 35 milionów zmarło.
Zapadalność na HIV na świecie osiągnęła szczyt w drugiej połowie lat 90., kiedy to w 1997 rozpoznano 3,7 miliona nowych zakażeń. Wśród zakażonych początkowo zdecydowanie dominowali mężczyźni, jednak liczba zakażeń wśród kobiet systematycznie rosła i obecnie kobiety stanowią blisko połowę osób zakażonych HIV.
W związku z wprowadzeniem programów profilaktycznych oraz leczenia antyretrowirusowego obserwuje się spadek liczby nowych zachorowań. Od 2010 obserwuje się coroczny spadkowy trend liczby nowych zachorowań, który dotyczy przede wszystkim osób poniżej 15 roku życia, a u osób powyżej 15 roku życia obserwuje się stabilizację liczby nowych zachorowań. Szacuje się, że liczba nowych zachorowań w 2015 wynosiła 2,1 miliona, przy czym 240 000 nowych przypadków odnotowano u dzieci poniżej 15 roku życia. W porównaniu do 2005 oznacza to spadek zapadalności o 35%.
Około połowy nowych zakażeń obserwuje się u osób w grupie wiekowej 15–24 lat. Choć spada liczba nowych zakażeń wśród dzieci i młodzieży poniżej 15 roku życia, nadal rozpoznaje się rocznie 240 000 nowych przypadków w tej grupie wiekowej i na świecie żyje 3,2 miliona dzieci zakażonych HIV. Obserwuje się wzrost populacji chorych powyżej 50 roku życia, której wielkość ocenia się na 4–4,5 miliona. Częściowo jest to związane ze zwiększeniem dostępności i skuteczności terapii antyretrowirusowej, która pozwala chorym dłużej żyć i osiągnąć 50. rok życia. Z drugiej strony znaczna część tej grupy chorych uległa zakażeniu już po 50 roku życia.
Liczba nowych zgonów z powodu zakażenia HIV ulega systematycznemu zmniejszeniu. W 2015 z powodu zakażenia HIV zmarło 1,1 miliona ludzi, choć w 2005 zanotowano 2 miliony zgonów, zatem od tego czasu umieralność uległa zmniejszeniu o 45%. Poprawia się dostępność do leczenia antywirusowego. Ma to związek z poprawą opieki zdrowotnej w krajach o niskich i średnich dochodach oraz spadku ceny tych leków. Jednak nadal tylko około połowa chorych (46%) na HIV otrzymuje leczenie antyretrowirusowe.
Do populacji o zwiększonym ryzyku zakażenia należą homoseksualni mężczyźni, osoby transseksualne, osoby świadczące usługi seksualne, osoby stosujące dożylne narkotyki oraz więźniowie. Rozmieszczenie geograficzne zakażenia wirusem HIV jest zróżnicowane, co jest związane z różnicami społecznymi i ekonomicznymi.
- Afryka Subsaharyjska
W Afryce Wschodniej i Południowej żyje 19 milionów osób zakażonych wirusem HIV, co stanowi 52% światowej populacji chorych. Również w tym regionie w 2015 stwierdzono 960 000 nowych zakażeń, co w przybliżeniu stanowi także połowę nowych zakażeń. Z kolei w Afryce Zachodniej i Centralnej żyje 6,5 miliona zakażonych, czyli około 18% światowej populacji, odnotowano również 410 000 nowych zakażeń. Obserwuje się trend spadkowy zapadalności oraz zgonów z powodu zakażenia HIV w tym regionie. Głównym wzorem transmisji zakażenia jest niezabezpieczony stosunek heteroseksualny. W dużym odsetku do zakażenia następuje u osób pozostających w stałym związku. Istotnym problemem jest transmisja matka–dziecko. Niemal 90% dzieci zakażonych wirusem HIV żyje w Afryce, choć liczba zakażeń w tej grupie wiekowej spada, to w 2013 zakażenie rozpoznano u 230 000 dzieci. Istnieją ograniczone dane dotyczące transmisji wirusa wśród mężczyzn mających kontakty seksualne z mężczyznami (MSM).
- Azja
Azja stanowi drugi region świata pod względem wielkości populacji chorych na HIV, najwięcej chorych żyje w Chinach i Indiach. W tym regionie żyje 5,1 miliona chorych i zanotowano 300 000 nowych przypadków HIV. Główną drogą transmisji w Chinach są kontakty heteroseksualne (46%) oraz dożylne przyjmowanie narkotyków (28,4%), w mniejszym stopniu za infekcje odpowiedzialne są kontakty homoseksualne pomiędzy mężczyznami. Za część przypadków odpowiada przetoczenie skażonego wirusem osocza w latach 90. W Indiach i Tajlandii istotną drogą transmisji jest korzystanie z usług pracowników seksualnych.
- Afryka Północna i Bliski Wschód
W Afryce Północnej i Bliskim Wschodzie obserwuje się stały, powolny wzrost liczby zachorowań i zgonów z powodu HIV. Szacuje się, że w tym regionie żyje 230 000 chorych i rocznie rozpoznaje się 20 000 nowych zachowań. Główną drogą transmisji wirusa jest dożylne przyjmowanie narkotyków oraz niezabezpieczony stosunek seksualny, w tym również homoseksualny.
- Ameryka Południowa, Łacińska i Karaiby
Liczba nowych zachorowań w Ameryce Łacińskiej i w regionie Karaibów pozostaje stabilna, ale ze względu na przyrost liczby chorych na HIV obserwuje się wzrost liczby zgonów związanych z tą chorobą. Ocenia się, że w tym regionie żyje 2 miliony chorych, w 2015 zanotowano 100 000 nowych zakażeń. Główną drogą transmisji jest stosunek bez zabezpieczenia. Bardzo wysoką częstość zakażenia obserwuje się wśród mężczyzn mający kontakty seksualne z mężczyznami (MSM), w niektórych obszarach Karaibów częstość zakażeń wśród MSM przekracza 25%. Ponadto wysoki odsetek zakażeń jest stwierdzany u osób transseksulanych, przyjmujących dożylnie narkotyki i pracowników seksualnych.
- Europa Wschodnia i Azja Środkowa
Obszar postradziecki jest regionem o szybko rosnącej populacji chorych na HIV, wrastającej liczby nowych zakażeń i zgonów z powodu zakażenia HIV. Na wzrost liczby zakażeń miały wpływ przemiany polityczne związane z rozpadem ZSRR powodujące spadek dochodów oraz niewydolność silnie scentralizowanej struktury opieki zdrowotnej. W tym regionie żyje około 1,5 miliona chorych na HIV, w 2015 stwierdzono 190 000 nowych zakażeń. Główną drogą transmisji jest dożylna podaż narkotyków. W Rosji 80% zakażeń tym wirusem rozpoznano u osób stosujących dożylne narkotyki. Rośnie na znaczeniu transmisja zakażenia na drodze stosunków heteroseksualnych. Zakażenia u mężczyzn mających kontakty seksualne z mężczyznami stanowią jedynie niewielki odsetek nowych zakażeń (<1%) w tym regionie świata.
- Europa Zachodnia, Środkowa i Ameryka Północna
Wśród krajów o wysokim dochodzie obserwuje się podobne trendy epidemiologiczne. Liczba nowych zakażeń pozostaje stabilna, w 2015 rozpoznano ich 91 000. Liczba zgonów z powodu HIV wykazuje tendencję spadkową i w 2015 zanotowano ich 22 000. Rośnie liczba żyjących chorych zakażonych wirusem HIV, których liczebność jest szacowana na 2,4 miliona. Największa częstość występowania zakażenia wśród krajów o wysokim dochodzie jest obserwowana w Estonii, Portugalii i Stanach Zjednoczonych. We wszystkich krajach Europy Zachodniej, Środkowej i Ameryki Północnej obserwuje się 2,5-krotnie częstsze występowanie zakażenia u mężczyzn, choć w niektórych krajach przewaga zakażeń u mężczyzn jest nawet 5,6-krotna. Zatem głównym wzorem transmisji są kontakty homoseksualne pomiędzy mężczyznami. Ważną drogą transmisji jest dożylne przyjmowanie narkotyków. W niektórych krajach jak Portugalii, Norwegii, Szwecji, Finlandii i Szwajcarii dominuje droga kontaktów heteroseksualnych. Część przypadków HIV w Europie Zachodniej jest stwierdzana u emigrantów z Afryki Subsaharyjskiej, podobnie w Stanach Zjednoczonych więcej przypadków odnotowuje się u Afroamerykanów.
- Polska
Polska należy do krajów o jednej z najniższej odnotowanej i szacowanej częstości zakażenia wirusem HIV. Od wprowadzenia rejestracji chorych w 1986 zanotowano łącznie blisko 21 tysięcy przypadków zakażenia HIV i 3400 przypadków AIDS. Początkowo w latach dziewięćdziesiątych epidemia HIV była związana z dożylnym przyjmowaniem narkotyków, od lat dwutysięcznych epidemia rozszerza się głównie w wyniku kontaktów homoseksualnych pomiędzy mężczyznami. Nadal większość dotychczas stwierdzonych zakażeń jest związana z dożylnym przyjmowaniem narkotyków, które jako drogę zakażenia przypisuje się 6 tysiącom przypadków zakażenia HIV. Z kolei u 2,9 tysiącom chorych zakażenie HIV jest związane z kontaktami homoseksualnymi, a u 1500 osób z kontaktami heteroseksualnymi.
Zakażenie HIV w Polsce zdecydowanie częściej jest rozpoznawane u mężczyzn, którzy stanowią 75–80% przypadków. W 2015 w Polsce zarejestrowano 1273 nowe zakażenia wirusem HIV, najczęstszą drogą zakażenia były kontakty homoseksualne mężczyzn (277 osób), kontakty heteroseksualne (90 osób) i dożylne przyjmowanie narkotyków (49 osób), ponadto rozpoznano cztery przypadki zakażenia dziecka przez matkę oraz jeden zakażenia jatrogennego. W 66,9% przypadków nie podano prawdopodobnej drogi zakażenia. W Polsce do nowych zakażeń u mężczyzn dochodziło najczęściej w wieku 20–29 lat, a u kobiet w przedziale wiekowym 30–39 lat.
Populacje kluczowe
Wyróżnia się kilka populacji o nieproporcjonalnie wysokim ryzyku zakażenia wirusem HIV. Do takich populacji należą mężczyźni mających kontakty seksualne z innymi mężczyznami, osoby transseksualne, pracownicy seksualni, osoby przyjmujące dożylnie narkotyki oraz więźniowie. W tych grupach obserwuje się marginalizację i stygmatyzację społeczną, przy jednoczesnej obecności zachowań zwiększających ryzyko zakażenia. W tych grupach stwierdza się ograniczoną dostępność do programów profilaktycznych i leczniczych, co sprzyja dalszemu szerzeniu się epidemii.
Transmisja wirusa
| Droga zakażenia | Oszacowane zakażenia na 10 000 ekspozycji na źródło zakażenia | |||
|---|---|---|---|---|
| Transfuzja krwi | 9250 | |||
| Poród | 2255 | |||
| Używanie tych samych igieł do wstrzykiwania narkotyków | 63 | |||
| Przezskórne ukłucie igłą | 23 | |||
| Bierny stosunek analny* | 138 | |||
| Czynny stosunek analny* | 11 | |||
| Stosunek pochwowy receptywny* | 8 | |||
| Stosunek pochwowy insertywny* | 4 | |||
| Stosunek oralny receptywny* | bardzo niskie | |||
| Stosunek oralny insertywny* | bardzo niskie | |||
| * zakładany brak użycia prezerwatywy | ||||
Do zakażenia wirusem HIV następuje poprzez kontakt seksualny, ekspozycję na wydzieliny lub tkanki zawierające wirusa oraz na drodze okołoporodowej (wertykalnej). Materiał potencjalnie zakaźny musi ulec kontaktowi z błoną śluzową (pochwy, odbytnicy, prącia, jamy ustnej) lub z uszkodzoną skórą albo zostać przeniesiony bezpośrednio do krwiobiegu. Materiałem zakaźnym jest krew, sperma, preejakulat, wydzielina pochwy, wydzielina z odbytu, mleko ludzkie i tkanki nieutrwalone formaliną. Do materiałów zakaźnych zalicza się również płyn mózgowo-rdzeniowy, płyn stawowy, płyn opłucnowy, płyn otrzewnowy i płyn osierdziowy, które stanowią potencjalne źródło wirusa, choć zakażenie za pośrednictwem tego materiału jest bardzo mało prawdopodobne. Ślina, plwocina, pot, łzy, mocz, kał i wymiociny, jeśli nie są zanieczyszczone krwią, nie są uważane za materiał zakaźny. Wirus HIV nie przenosi się poprzez owady, w tym również komary, kleszcze i moskity. HIV również nie przenosi się poprzez dotyk, uścisk dłoni, przytulanie, współdzielenie toalety czy kuchni, a także wspólne spożywanie posiłków.
Na ryzyko zakażenia wpływ ma typ materiału potencjalnie zakaźnego, poziom wiremii HIV w materiale, rodzaj ekspozycji i współistnienie chorób przenoszonych drogą płciową.
Droga seksualna jest najważniejszą drogą transmisji wirusa, ogólnie pośredniczy ona w dwóch trzecich przypadków zakażenia. Ryzyko zakażenia różni się w zależności od rodzaju aktywności seksualnej. Największe ryzyko wiąże się ze stosunkiem analnym biernym (receptywnym). W porównaniu do receptywnego kontaktu waginalnego receptywny kontakt analny wiąże się z ponad dziesięciokrotnie większym ryzykiem infekcji. Większe ryzyko jest związane z ekspozycją bogatounaczynionej błony śluzowej odbytnicy z nasieniem zawierającym wysoką koncentrację wirusa. Ocenia się, że ryzyko zakażenia HIV w kontakcie analnym receptywnym wynosi 138 na 10 000 przypadków ekspozycji.
Z mniejszym ryzykiem w porównaniu do stosunku analnego biernego wiąże się z stosunek analny aktywny (insertywny). Ryzyko jest związane z ekspozycją na zawierającą wirusa HIV krew w odbytnicy. Szacuje się, że ryzyko zakażenia wynosi około 11 przypadków na 10 000 przypadków ekspozycji. Stosunek dopochwowy zarówno receptywny, jak insertywny niesie znacznie mniejsze ryzyko zakażenia niż stosunek analny, co jest związane z mniejszym prawdopodobieństwem krwawienia podczas stosunku dopochwowego. Ocenia się, że receptywny stosunek waginalny wiąże się z 8 przypadkami zakażenia na 10 000 przypadków ekspozycji, a insertywny stosunek dopochwowy z 4 przypadkami zakażenia na 10 000 przypadków ekspozycji. Ryzyko zakażenia podczas stosunku oralnego jest znacznie niższe niż podczas stosunku analnego czy dopochwowego, jednak precyzyjne określenie ryzyka zakażenia jest trudne. Prawdopodobnie receptywne fellatio wiąże się z większym ryzykiem niż inne formy seksu oralnego, w tym cunnilingus czy anilingus. Uważa się, że jama ustna bez zmian chorobowych stanowi dobrą barierę chroniącą przed zakażeniem HIV. Choć niewielka liczba prac wskazuje na obecność wirusa HIV w ślinie, to nie ma dowodów na transmisję zakażenia poprzez ślinę. Ponadto w ślinie obecne są enzymy oraz przeciwciała inaktywujące wirusa.
Przy przypadkowym zakłuciu igłą zanieczyszczoną materiałem zakaźnym wynosi 0,23%. Faktyczna wielkość ryzyka zależy od głębokości zakłucia, obecności krwi w świetle igły i poziomu wiremii. Wirus jest dość podatny na wysuszanie, choć może przetrwać w strzykawce do 42 dni. Poza zakłuciem igłą u pracowników ochrony zdrowia (jako narażenie zawodowe) rzadko dochodzi do zakłucia igłą świeżo po użyciu, a igła rzadko zawiera świeżą krew. Prawdopodobieństwo zakażenia wirusem HIV poprzez igły porzucone w miejscu publicznym jest bardzo niskie, dotyczy przede wszystkim igły zawierającej świeżą krew. Stosowanie tych samych igieł do wstrzykiwania narkotyków wiąże się ze znacznie większym ryzykiem, które jest oceniane na 63 przypadków na 10 000 przypadków ekspozycji. Indywidualne ryzyko związane z używaniem tych samych igieł do wstrzykiwania narkotyków zwiększa biesiadne używanie narkotyków, odbywanie kary pozbawienia wolności, stosowanie kokainy lub opiatów oraz marginalizacja społeczna.
Transfuzja zakażonej krwi lub preparatów krwiopochodnych jest najefektywniejszą drogą transmisji wirusa. Zdecydowaną większość zakażeń poprzez transfuzję zanotowano przed 1985 rokiem, kiedy to wprowadzono przesiewowe badanie dawców krwi w kierunku wirusa HIV. W Polsce serologiczne badania przesiewowe w kierunku HIV zostały wprowadzone już w 1986. Postęp technik diagnostycznych badań serologicznych i wprowadzeniem technik molekularnych do diagnostyki dawców pozwoliło znacznie zmarginalizować ryzyko zakażenia drogą transfuzji krwi i dodatkowo podniosło bezpieczeństwo transfuzji. W Polsce w badaniu dawców stosuje się badania immunoenzymatyczne (EIA) wykrywających przeciwciała anty-HIV i białko wirusa p24 oraz badania RT-PCR wykrywającego materiał genetyczny wirusa. Obecnie ryzyko zakażeniem wirusem HIV poprzez transfuzję krwi jest bardzo niskie i w różnych publikacjach jest ocenianie na 0,14–1,5 przypadków zakażenia na 1 000 000 przetoczeń.
Do zakażenia wirusem HIV z matki na dziecko (zakażenie wertykalne) może nastąpić wewnątrzłożyskowo, podczas porodu i karmienia piersią. Ryzyko zakażenia wertykalnego bez profilaktyki jest oceniane na 2255 przypadków na 10 000 przypadków ekspozycji. W wewnątrzmacicznej transmisji wirusa przez łożysko pośredniczą komórki śródbłonka zawierające receptor CD4 oraz komórki Hofbauera. Zakażenie podczas porodu jest związane z ekspozycją noworodka na krew, płyn owodniowy oraz wydzielinę dróg rodnych. Profilaktyka zakażenia wertykalnego polega na przyjmowaniu przez matkę HAART, wykonaniu planowego (elektywnego) cięcia cesarskiego, podania dożylnie zydowudyny w trakcie porodu oraz profilaktyczne włączenie noworodkowi leków antyretrowirusowych. Wdrożenie profilaktyki za pomocą zydowudyny zmniejszyło ryzyko zakażenia wertykalnego do 8,3%, obecnie dzięki wprowadzeniu HAART ryzyko zakażenia wertykalnego spada do 1–2%. Planowe cięcie cesarskie również sprzyja redukcji ryzyka transmisji HIV i jest wykonywane na dwa tygodnie przed przewidywanym terminem porodu.
Udowodniono, że u osób z HIV skutecznie leczonych terapią przeciwwirusową nie istnieje ryzyko przeniesienia HIV na inne osoby (U=U).
Patogeneza
Cykl replikacyjny wirusa HIV
Cykl życiowy wirusa HIV wymaga wykorzystania komórki gospodarzowej. W replikacji kluczową rolę pełnią glikoproteina błonowa gp120 połączona z przezbłonową glikoproteiną gp41 oraz receptor komórkowy CD4. Receptor CD4 występują przede wszystkim na powierzchni limfocytów pomocniczych Th, ale także komórek prekursorowych T w szpiku i grasicy, komórkach dendrytycznych, makrofagach, monocytach, eozynofilach i komórkach mikrogleju. Replikacja wirusa HIV rozpoczyna przyłączenie wirusowej glikoproteiny gp120 ze swoim receptorem komórkowym CD4+ przy udziale koreceptorów.
Połączenie gp120 z CD4 wywołuje kaskadę zmian komformacyjnych gp120 i odsłonięcia miejsca wiązania gp120 z koreceptorami. Udział koreceptorów jest niezbędny do zakażenia komórki gospodarzowej; podstawowymi koreceptorami są prawidłowe receptory dla chemokin – CCR5 (receptor β-chemokin) oraz CXCR4 (receptor α-chemokin). Po związaniu gp120 z koreceptorami dochodzi do dalszych zmian komformacyjnych gp120 i zostaje odsłonięta hydrofobowa domena gp41 zbudowana z sześciu powiązanych z sobą spiralnych podjednostek, która następnie zostaje wprowadzona do błony komórki gospodarzowej. Dochodzi do połączenia i fuzji osłonki wirusowej z błoną komórkową, a następnie przemieszczenia otoczonego przez kapsyd RNA wirusa do cytoplazmy komórki gospodarzowej.

(1) Wstępna interakcja pomiędzy wirusem HIV a komórką gospodarzową
(2) Zmiana komformacji gp120 umożliwiającą interakcję z koreceptorem
(3) Hydrofobowe domeny gp41 są wprowadzane do błony komórki gospodarzowej
(4) Dalsze zmiany komformacyjne i połączenie osłonki wirusowej z błoną komórki gospodarzowej

Po uwolnienie z kapsydu RNA wirusa ulega odwrotnej transkrypcji. W tym procesie przy udziale enzymu odwrotnej transkryptazy (RT) na podstawie nici wirusowego RNA najpierw powstaje komplementarna nić DNA, a następnie druga nić i dwuniciowy DNA. W trakcie tego mogą powstawać liczne mutacje i nowe warianty wirusa ponieważ odwrotna transkryptaza nie posiada zdolności korekcji błędów. HIV DNA posiada na obu końcach regiony LTR, które zawierają miejsca inicjacji transkrypcji.
Powstały w procesie odwrotnej transkrypcji HIV DNA w obrębie cytoplazmy jest ściśle związany w białkami wirusowymi, jak integraza, odwrotna transktyptaza i białkami nukleokapsydu, oraz białkami komórki gospodarzowej, jak Ku, INI 1 czy HMGa1 – razem tworzą one kompleks przedintegracyjny. Powstały w procesie odwrotnej transkrypcji kompleks przedintegracyjny (PIC) jest transportowany do jądra komórkowego, gdzie integraza rozpoznaje sekwencje nukleotydowe zlokalizowane na końcach regionów LTR U3 oraz U5 w wirusowym DNA i katalizuje włączenie go do chromosomu gospodarzowego.
W regionie LTR znajdują się elementy regulujące transkrypcję wirusowego DNA, obecny jest wzmacniacz transkrypcji z motywem wiążącym NF-κB, NFAT, promotor wiążący Sp1 oraz sekwencja TATA. Zatem transkrypcja wirusowego DNA zostaje powiązana z sygnałami aktywującymi komórkę, takimi jak cytokiny, biorącym w prezentacji antygenu TCR, które powodują przesunięcie NF-κB lub NFAT z cytoplazmy do jądra komórkowego. Wydajność transkrypcji znacząco zwiększa białko wirusowe tat.
Proces transkrypcji jest regulowany w czasie za pośrednictwem procesu splicingu mRNA oraz białek tat i rev. Pełny transkrypt wirusowego genomu posiada 9 kb (posiada również geny gag, pol i env), przy czym w procesie splicingu powstaje mRNA z 2 kb zawierające wyłącznie gen tat, rev i nef oraz mRNA z 4 kb posiadające geny Env, Vif, Vpr, Vpu. Początkowo w procesie transkrypcji powstaje białko tat, które zwiększa wydajność transkrypcji, a następnie powstaje białko rev regulujące powstawanie białek strukturalnych i enzymatycznych. W wyniku oddziaływania białka rev dochodzi do eksportu RNA niepoddane procesowi splicingu (pre-mRNA) lub częściowemu splicingowi z jądra komórkowego do cytoplazmy, gdzie ulega ono translacji. W przypadku niewystarczająco wysokiej ekspresji rev niepoddane splicingowi RNA pozostaje w jądrze komórkowym i ulega degradacji. Białka strukturalne kodują geny gag, pol i env. W wyniku działania proteazy z białek prekursorowych kodowanych przez geny pol i env powstają p17 (białko macierzy), p24 i nukleoproteiny p9 i p7. Gen env koduje glikoproteinę gp160, która w aparacie Golgiego pod wpływem proteaz komórkowych jest przekształcana w gp120 i gp41, które wędrują do błony komórki gospodarzowej w celu sformowania wirionu. Wirusowe RNA dimeryzuje i zostaje zapakowane do wirionu. W procesie pączkowania powstaje wirion, przy czym w trakcie tego procesu do własnej osłonki wirusowej HIV włącza błonowe białka komórki gospodarzowej, w tym MHC, cząsteczki adhezyjne i inhibitory dopełniacza. Włączenie tych białek zwiększa infekcyjność wirusa i nasila aktywację immunologiczną. Wirion jest uwalniany w wyniku lizy komórki gospodarzowej.
Komórkowe mechanizmy obronne
Komórki posiadają kilka mechanizmów obronnych działających na wielu etapach cyklu replikacyjnego wirusa. TRIM5α wpływa na przedwczesne rozłożenie osłonki wirusowej, zniszczenie kapsydu i zatrzymanie odwrotnej transkryptazy. APOBEC3G poprzez dezaminację deoksycytydyny do deoksyurydyny w ujemnej nici prowirusowego DNA, co ostatecznie przerywa cykl życiowy wirusa na etapie odwrotnej transkryptazy. SAMHD1 hydrolizuje dNTPs zmniejszając jego dostępność dla odwrotnej transkryptazy.
Pierwotne zakażenie HIV
Okres od wniknięcia wirusa do czasu wytworzenia przeciwciał anty-HIV jest nazywany pierwotnym zakażeniem HIV. Większość świeżych zakażeń jest spowodowanych przez wirusy CCR5-tropowe, a wirusy CXCR4-tropowe pojawiają się w późniejszych fazach zakażenia. Po wniknięciu HIV w blaszce właściwej błony śluzowej następuje zakażenie niewielkiej liczby komórek dendrytycznych, limfocytów CD4+ oraz makrofagów. Potencjalnymi drogami inwazji może być endocytoza, transcytoza lub przyłączenie do receptorów mammozy (DC-SIGN), które są obecne na komórkach dendrytycznych i makrofagach.
Klasyczną drogę rozprzestrzeniania się wirusa stanowi bezpośrednie zakażenie komórek docelowych przez wolny wirus. Jednak wirus może wykorzystywać prawidłowe mechanizmy prezentacji antygenu do dalszego rozprzestrzeniania. Bezpośrednia transmisja w ramach synapsy immunologicznej pomiędzy komórką dendrytyczną a limfocytem CD4+ jest skuteczniejszą metodą zakażania kolejnych komórek i w modelach matematycznych stanowi drogę nawet 90% nowych zakażeń w tkance limfatycznej.
Komórka dendrytyczna jest komórką prezentującą antygen (APC). Komórki dendrytyczne prezentują antygen związany z cząstką MHC receptorowi komórki T (TCR), co prowadzi do stymulacji tych komórek. Komórki dendrytyczne wyrażają ekspresję niewielkich ilości receptorów CD4, znaczną ilość receptorów CCR5 i CXCR4 oraz szereg innych receptorów pośredniczących w wiązaniu z wirusową gp 120, w tym DC-SIGN i DCIR, ponadto posiadają zdolność do makropinocytozy chwytając całe antygeny i patogeny. Po związaniu z receptorem dalsze losy związanego wirusa HIV zależą od rodzaju receptora oraz stopnia dojrzałości i interakcji komórki dendrytycznej. Komórki dendrytyczne pomimo posiadania receptorów CD4 w porównaniu do limfocytów CD4+ są stosunkowo rzadko zakażane. Związanie HIV z DC-SIGN nie prowadzi do jego pełnej degradacji, a do zatrzymania go w endosomach. Po wniknięciu wirusa HIV może on ulegać degradacji i przygotowaniu do prezentacji antygenu limfocytom CD4+. Wirus zatrzymany w endosomach, który nie uległ degradacji, wraz z uwalnianiem pęcherzyków z wirusem jest może ponownie przedostać się do otoczenia i dalej łączyć się z komórkami docelowymi. Komórka dendrytyczna z obecnym na jej powierzchni wirusem HIV indukuje rekrutację CD4, CCR5, CXCR4 na powierzchni limfocytów CD4+ i tworzy analogiczną strukturę do synapsy immunologiczną nazywaną synapsą zakaźną. Powstanie synapsy zakaźnej wymaga udziału białek adhezyjnych typowo wykorzystywanych podczas fizjologicznej interakcji pomiędzy tymi komórkami. Następnie dochodzi do uwolnienia wirionów w strefie styku obu komórek i zakażenia komórki docelowej. Zdolność do migracji i możliwość interakcji z wieloma limfocytami Th zwiększa znaczenie takiej drogi rozprzestrzenia wirusa.
Po zakażeniu komórek dendrytycznych, limfocytów CD4+ oraz makrofagów lub jako wolny wirion wirus HIV wędruje do lokalnych węzłów chłonnych. Po około tygodnia od zakażenia w regionalnych węzłach chłonnych następuje replikacja wirusa, która pozwala na zwiększenie liczby wirusów o niewielkiej liczbie wariantów. Następnie w ciągu 1–3 tygodni od zakażenia zakażone limfocyty T wędrują drogą krwionośną i docierają do przewodu pokarmowego, szpiku oraz śledziony, gdzie następnie dochodzi do intensywnej replikacji i masywnego zakażenia komórek wrażliwych. Skutkuje to bardzo wysokim poziomem wiremii we krwi. Wysoki poziom replikacji skutkuje znacznym obniżeniem liczby limfocytów CD4+, szczególnie w obrębie błony śluzowej przewodu pokarmowego, gdzie w ciągu 3 tygodni ginie ponad 80% limfocytów CD4+. Spadek liczby limfocytów CD4+ w obrębie jelita jest nieodwracalny i może skutkować przesunięciem drobnoustrojów do krwiobiegu, co sprzyja aktywacji immunologicznej. Obserwuje się znaczny spadek liczby komórek pamięci o fenotypie CD4+CD45Ro+.
Swoiste limfocyty cytotoksyczne CD8+ likwidują zakażone komórki prowadząc do gwałtownego spadku wiremii, ale nie doprowadzając do eradykacji zakażenia. Limfocyty CD8+ prowadzą do zmniejszenia wiremii w wyniku niszczenia zakażonych komórek oraz poprzez hamowanie replikacji bez niszczenia zakażonych komórek. Dochodzi do wytwarzania perforyny, indukcji apoptozy poprzez połączenie ligandu Fas z receptorem Fas oraz produkcję INF-γ i CAF. Inną funkcją limfocytów CD8+ jest wytwarzanie chemokin CCL3, CCL4 i CCL5, które konkurują z receptorem CCR5. Ustala się pewien poziom wiremii nazywany punktem ustalenia, który ma wpływa na dalszy przebieg infekcji.
W ciągu 3–4 tygodnia od zakażenia pojawiają się swoiste przeciwciała anty-HIV. Większość przeciwciał jest skierowana przeciw glikoproteinom otoczkowym gp 41 i gp 120. Przeciwciała mogą prowadzić do zablokowania infekcji komórek docelowych (przeciwciała neutralizujące) lub nakierowywać inne komórki układu immunologicznego na zniszczenie zakażonych komórek. Jednak powstałe przeciwciała mają niewielki wpływ neutralizujący na obecne antygeny wirusowe. Zakres rozpoznawanych przez przeciwciała epitopów jest wąski. Rzadko dochodzi do powstania swoistych przeciwciał przeciwko konserwatywnym regionom glikoprotein powierzchniowych, a jeśli się pojawiają to najczęściej dopiero po 20–30 miesiącach infekcji.
Przewlekłe zakażenie HIV

Poziom wiremii
Poziom limfocytów CD4+
Po około 6 miesiącach od infekcji zakażenie wchodzi w okres bezobjawowy. Typową cechą przewlekłego zakażenia jest przewlekła aktywacja immunologiczna i postępujący spadek liczby limfocytów CD4+. Obniżenie ich liczby wynika bezpośrednio z zakażenia tych komórek HIV oraz apoptozy zakażonych i niezakażonych limfocytów CD4+.
Aktywacja immunologiczna
Stała, nieswoista aktywacja immunologiczna jest kluczowym elementem patogenezy zakażenia silnie nasilającym replikację wirusa i ostatecznie indukującym wyczerpywanie puli komórek immunologicznych. U podstaw stałej aktywacji immunologicznej leży sama replikacja wirusa i odpowiedź immunologiczna na zakażenie oraz translokacja mikroorganizmów z przewodu pokarmowego. Mechanizm prowadzący do przewlekłej aktywacji immunologicznej jest złożony i nie do końca poznany, prawdopodobnie udział różnych mechanizmów składających się na ten proces różni się u poszczególnych chorych w zależności od etapu infekcji oraz stosowania HAART.
Do aktywacji immunologicznej prowadzi sama replikacja wirusa i odpowiedź immunologiczna na zakażenie. Wirus jest rozpoznawany przez swoiste receptory TCR, ale także jest wiązany przez receptor toll-podobny. HIV, zakażając limfocyty CD4+, może jednocześnie aktywować zakażone komórki. Choć poziom replikacji HIV koreluje z aktywacją immunologiczną i stanem zapalnym, nie jest jedynym czynnikiem wyzwalającym proces utrwalonej aktywacji immunologicznej, o czym świadczy zaangażowanie w proces aktywacji i zwiększonego obrotu innych komórek niż limfocyty CD4+ oraz brak ustąpienia procesu po skutecznym leczeniu antyretrowirusowym. Kolejnym mechanizmem, szczególnie istotnym w zaawansowanych stadiach zakażenia, są infekcje oportunistyczne i nieoportunistyczne. Patogeny poprzez stymulację dużej liczby komórek promują i podtrzymują stałą aktywację. Procesowi sprzyja utrata limfocytów Th17, utrata integralności błony śluzowej przewodu pokarmowego i przesunięcie flory jelitowej oraz jej antygenów, w tym lipopolisacharydu (LPS), do krwiobiegu.
Stała aktywacja immunologiczna istotnie przyczynia się do progresji choroby. Prowadzi ona do aktywacji i proliferacji limfocytów CD4+ naiwnych i pamięci ze zwiększeniem ekspresji receptorów CCR5, które zwiększają podatność na infekcję HIV. Paradoksalnie zwiększona proliferacja limfocytów CD4+ zwiększa liczbę komórek docelowych dla wirusa, a aktywacja limfocytów CD4+ sprzyja replikacji wirusa, co napędza błędny cykl. Stała aktywacja zaburza funkcję limfocytów B, komórek NK, komórek dendrytycznych i monocytów, czego skutkiem jest gorsza kontrola infekcji i dalsze nasilenie procesu. Kolejnym następstwem stałej aktywacji układu immunologicznego jest deregulacja funkcji szpiku kostnego, grasicy i węzłów chłonnych. W wyniku przewlekłej produkcji TGF-β1 dochodzi do uszkodzenia komórek fibroblastycznych siateczki i tworzonych przez te komórki sieć, spada dostępność IL-7, co zmniejsza zdolność do przetrwania naiwnych limfocytów T. Uszkodzenie sieci komórek fibroblastycznych siateczki ogranicza rekonstrukcję układu immunologicznego po wprowadzeniu leczenia antyretrowirusowego. Indukowane przez stała aktywność immunologiczną uszkodzenie naczyń i zaburzenia lipidowe promują choroby sercowo-naczyniowe. Stymulacja proliferacji komórek nowotworowych sprzyja rozwojowi nowotworów niedefiniujących AIDS
Apoptoza limfocytów CD4+
Początkowo podczas ostrej fazy zakażenia spadek liczby limfocytów CD4+ jest związany z wysoką wiremią. Wirus preferencyjnie infekuje limfocyty swoiste dla wirusa. W fazie przewlekłej głównym mechanizmem utraty limfocytów CD4+ jest apoptoza.
Do śmierci zakażonej komórki może dochodzić w wyniku cytolizy bezpośrednio związanej z zakażeniem i cyklem replikacyjnym wirusa, a także w wyniku zniszczenia komórki przez limfocyty cytotoksyczne CD8+. Do apoptozaly niezakażonych komórek przyczynia się białko Env (gp 120 i gp 41). Komórki wykazujące ekspresję Env wiążąc się z CD4 i CXCR4/CCR5 obecnymi na niezakażonych komórkach mogą tworzyć syncytia lub częściowe wymieszanie się błon komórkowych, co skutkuje zniszczeniem tych komórek.
Większość limfocytów CD4+ jest niszczona w pośrednim mechanizmie, przede wszystkim śmierci komórkowej indukowanej aktywacją (AICD, od ang. activation-induced cell death) związanej z procesem przewlekłej aktywacji immunologicznej. Fizjologicznie regulacja odpowiedzi immunologicznej i jej wygaszanie wymaga uśmiercenia znacznej części już niepotrzebnych limfocytów biorących udział w tej odpowiedzi. W tej regulacji uczestniczą cząsteczki Fas i nadrodzina TNF. Przewlekłej aktywacji immunologicznej towarzyszy wzrost ekspresji ligandów i receptorów nadrodziny TNF – Fas/FasL and TRAIL-DR5. Cząstka FasL jest wyrażana tylko w niewielkich ilościach przez naiwne limfocyty T, ale w aktywowanych limfocytach jego ekspresja jest znaczna. Zakażone komórki znacznie w mniejszym stopniu ulegają apoptozie niż te niezakażone i skutkuje to oszczędzeniem zainfekowanych limfocytów, przy jednoczesnym niszczeniu aktywowanych komórek.
Niszczenie niezakażonych komórek jest również związane z białkami wirusowymi gp120, Tat i Nef. Gp 120 wiążąc się CD4 i koreceptorami prowadzi do regulacji w górę Fas i obniżenia FLIP, który jest inhibitorem kaspazy 8, co kieruje komórkę na szlak wewnątrzpochodny apoptozy. Z kolei Tat reguluje w górę TRAIL, a Nef w różnych mechanizmach kieruje komórkę na szlak wewnątrzpochodny i zewnątrzpochodny apoptozy.
Zmienność genotypowa HIV
HIV cechuje się wyjątkowo nasiloną zdolnością do akumulacji zmienności genetycznej. Prowadzi to znacznego zróżnicowania obecnych populacji HIV u zakażonego. Źródłem zmienności genetycznej jest przede wszystkim podatność na błędy wirusowej odwrotnej transkryptazy, ale także białka gospodarza – polimerazę RNA II (Pol II) i ABOBEC3G (dezaminazę cytydyny). Ocenia się, że podczas replikacji dochodzi do pojedynczego błędu na 104–105 nukleotydów, czyli powstaje jedna mutacja na replikację całego materiału genetycznego. Przekłada się to na 1010 mutacji dziennie. Pozwala to na selekcję wielu wariantów wirusa mających określone korzystne cechy lub zdolność do ucieczki od odpowiedzi układu immunologicznego gospodarza, a także do oporności na leki antyretrowirusowe. Mutacje w zakresie rozpoznawanych przez limfocyty CD8+ epitopy umożliwiają uniknięcie zniszczenia i dają korzyść selekcyjną nowym wariantom wirusa. Glikoproteiny env w pętlach hiperzmiennych V1, V2 i V4, poza mutacjami punktowymi, wykazują zmiany strukturalne powodujące wydłużenie tych pętli ze zwiększeniem miejsc glikozylacji. Mutacje prowadzące do oporności na leki pojawiają się jeszcze przed wprowadzeniem tych leków, następnie w wyniku działania presji selekcyjnej (zastosowany lek) dochodzi do wzrostu opornych populacji wirusa. W konsekwencji tego zjawiska leczenie za pomocą pojedynczego leku zawsze prowadzi do szybkiego nawrotu wiremii klonów opornych na ten lek.
Faza objawowa – zespół nabytego niedoboru odporności
Faza objawowa jest następstwem znacznego upośledzenia czynnościowego układu odpornościowego i dalszej szybkiej progresji choroby. Wczesna faza objawowa może pojawiać się przy spadku liczby limfocytów CD4+ poniżej 500 komórek/μl. Przy spadku liczby limfocytów CD4+ poniżej 200 komórek/μl mogą się pojawiać infekcje, nowotwory i inne choroby wskaźnikowe AIDS. Często rozpoznawanymi infekcjami oportunistyczni są gruźlica, mykobakteriozy, Pneumocystis carinii i cytomegalia. Do zgonu dochodzi w wyniku zakażeń lub niewydolności życiowo istotnych narządów, szczególnie w przebiegu niewydolności oddechowej, niewydolności krążenia, niewydolności hematopoezy lub uszkodzenia ośrodkowego układu nerwowego.
Obraz kliniczny zakażenia HIV
| Kategoria immunologiczna | Kategoria kliniczna | ||
| Liczba limfocytów CD4+ | A | B | C |
| Faza bezobjawowa, OChR lub PGL | Faza objawowa bez chorób wskaźnikowych AIDS | Choroby wskaźnikowe AIDS | |
| >500/μl | A1 | B1 | C1 |
| 200–499/μl | A2 | B2 | C2 |
| <200/μl | A3 | B3 | C3 |
| AIDS jest definiowany przez kategorie A3, B3, C1, C2 i C3 | |||
Kategoria kliniczna A – zakażenie bezobjawowe, ostra choroba retrowirusowa i przewlekła limfadenopatia uogólniona
- Ostra choroba retrowirusowa
U części chorych w ostrej fazie zakażenia obserwuje się chorobę o niecharakterystycznym przebiegu nazywaną ostrą chorobą retrowirusową. Ostra choroba retrowirusowa pojawia się między 1. a 8. tygodniem od zakażenia, najczęściej pomiędzy 3. a 6 tygodniem od zakażenia HIV. Choroba retrowirusowa cechuje się pewną zmiennością obrazu klinicznego. Może przybierać przebieg bezobjawowy lub objawowy przypominając mononukleozę zakaźną, grypę albo przeziębienie.
Przebieg objawowy ostrej choroby retrowirusowej jest obserwowany u 40–90%. Możliwy jest przebieg pod postacią jedynie stanu podgorączkowego trwającego kilka dni. Najczęstszymi objawami są gorączka, utrata apetytu i złe samopoczucie, które występują u ponad 70% chorych. Może występować silny ból głowy, zapalenie gardła, ból mięśni i ból stawów, biegunka, nudności, wymioty i utrata masy ciała. U części chorych występuje wysypka plamisto-grudkowa, najbardziej zaznaczona na twarzy i tułowiu, często obejmująca dłonie i stopy. W obrębie błony śluzowej jamy ustnej, narządów płciowych, odbytu i przełyku mogą być obecne ostro ograniczone owrzodzenia. W badaniu fizykalnym mogą być obecne uogólnione powiększenie węzłów chłonnych (limfadenopatia), szczególnie zaznaczona w obrębie grupy węzłów pachowych, szyjnych i potylicznych, a także powiększenie wątroby i śledziony.
Rzadko dochodzi do aseptycznego zapalenia opon mózgowo-rdzeniowych z niewielką pleocytozą z przewagą limfocytów, podwyższeniem stężenia białka i prawidłowym stężeniem glukozy, a bardzo rzadko zapalenie mózgu, neuropatii obwodowej i zespołu Guillaina-Barrégo. Bardzo rzadko w przebiegu ostrej choroby retrowirusowej dochodzi do rozwoju typowych infekcji oportunistycznych. W badaniach laboratoryjnych bywa obecna łagodna niedokrwistość, leukopenia, małopłytkowość i wzrost stężenia aminotransferaz (AST, ALT). Choroba zwykle samoistnie ustępuje w ciągu 7–10 dni, ale złe samopoczucie, powiększenie węzłów chłonnych i owrzodzenia mogą utrzymywać się kilka miesięcy.
- Zakażenie bezobjawowe
Niezależnie od rozwoju ostrej choroby retrowirusowej po ostrej fazie zakażenia pojawia się okres bezobjawowy zakażenia HIV. Okres klinicznie bezobjawowy trwa przeciętnie 8–10 lat. W tym okresie dochodzi do replikacji wirusa oraz do stałego, powolnego zmniejszania się liczby limfocytów CD4+ i postępującego pogorszenia funkcji układu odpornościowego.
- Przewlekłe uogólnione powiększenie węzłów chłonnych
W okresie poprzedzającym rozwój okresu objawowego zakażenia HIV może dochodzić do powstania przewlekłego uogólnionego powiększenia węzłów chłonnych (persistent generalized lymphadenopathy – PGL). Zespół jest definiowany przez stwierdzenie powiększenia co najmniej dwóch grup węzłów chłonnych poza węzłami pachwinowymi, o wielkości powyżej 1 cm, trwającego przynajmniej 3 miesiące po wykluczeniu innych przyczyn powiększenia węzłów chłonnych. Przewlekłe uogólnione powiększenie węzłów chłonnych występuje u 50–70% chorych zakażonych HIV.
Najczęściej powiększeniu ulegają węzły szyjne, podżuchwowe, potyliczne, pachowe, łokciowe, podkolanowe oraz krezkowe. Powiększenie węzłów śródpiersia nie jest typowe dla PGL. U co trzeciego chorego występuje również powiększenie śledziony. Powiększeniu ulegają symetryczne grupy węzłów, węzły są ruchome, sprężyste i zwykle niebolesne, wielkości około 0,5–2 cm. Asymetryczne i szybkie powiększenie węzłów nie jest typowe dla przewlekłego uogólnionego powiększenia węzłów chłonnych. Przewlekłemu uogólnionemu powiększeniu węzłów chłonnych mogą towarzyszyć infekcje patogenami nieoportunistycznymi, ból głowy i przewlekłe zmęczenie.
Przewlekłe uogólnione powiększenie węzłów chłonnych poprzedza wystąpienie okresu objawowego. Powiększenie węzłów chłonnych jest związane z intensywnym namnażaniem wirusa po pierwotnym zakażeniu HIV. Zanik powiększenia węzłów chłonnych wiąże się progresją zakażenia HIV. Historia naturalna zakażenia HIV nie różni się u chorych, u których wystąpiło PGL od tych, u których ono nie wystąpiło.
Kategoria kliniczna B – stadium objawowe bez zakażeń definiujących AIDS (nie-A i nie-C)
W tym stadium występują zakażenia oportunistyczne sugerujące niedobór odporności komórkowej, jednak nie spełniające kryteriów chorób wskaźnikowych AIDS. Zakażenia zwykle nadal przyjmują łagodny przebieg. Do zakwalifikowania do kategorii B decyduje stwierdzenie choroby związanej z zakażeniem HIV lub wskazującej na niedobory odpowiedzi komórkowej, a także stwierdzenie choroby, których przebieg lub wymagane leczenie komplikuje zakażenie HIV.
Do typowych stanów związanych ze stadium objawowym bez zakażeń definiujących AIDS (kategoria B) zalicza się:
- angiomatozę bakteryjną
- leukoplakię włochatą
- półpasiec obejmujący powyżej jednego dermatomu lub ponowne wystąpienie półpaśca
- kandydozę jamy ustnej i kandydozę pochwy
- zapalenie narządów miednicy mniejszej
- dysplazję szyjki macicy lub rak in situ szyjki macicy
- małopłytkowość immunologiczną
- listeriozę
- neuropatię obwodową
- gorączkę powyżej 38,5 °C lub biegunkę powyżej jednego miesiąca.
Kategoria kliniczna C – pełnoobjawowe AIDS
AIDS jest rozpoznawany w konsekwencji stwierdzenia dowolnej choroby wskaźnikowej (definiującej AIDS), do których należą zakażenia oportunistyczne, nowotwory oraz inne zespoły chorobowe etiologicznie ściśle związane z zakażeniem HIV. AIDS jest również rozpoznawane u chorych zakażonych HIV z liczbą limfocytów CD4+ poniżej 200 komórek/μl, przy czym kliniczne pojawienie się AIDS jest prawdopodobne przy obniżeniu liczby limfocytów CD4+ poniżej 400–200 komórek/μl.
Choroby wskaźnikowe AIDS:
- zakażenia oportunistyczne:
- nawracające, bakteryjne zapalenia płuc (przynajmniej 2 zachorowania w ciągu 12 miesięcy)
- gruźlica płucna lub pozapłucna
- mykobakterioza rozsiana lub pozapłucna
- nawracająca uogólniona salmonelloza
- kandydoza przełyku, tchawicy, oskrzeli lub płuc
- pneumocystozowe zapalenie płuc
- histoplazmoza pozapłucna
- kokcydioidomykoza pozapłucna
- kryptokokoza pozapłucna
- izosporoza
- toksoplazmoza narządowa
- kryptosporydioza
- węgorczyca pozajelitowa
- przewlekłe owrzodzenia skóry i (lub) błon śluzowych, utrzymujące się ponad miesiąc, zapalenie oskrzeli, płuc lub przełyku spowodowane przez HHV
- cytomegalia (poza wątrobą, śledzioną i węzłami chłonnymi)
- postępująca wieloogniskowa leukoencefalopatia (PML)
- nowotwory:
- mięsak Kaposiego u mężczyzny poniżej 60 roku życia
- chłoniaki: Burkitta, pierwotny mózgu, immunoblastyczny
- inwazyjny rak szyjki macicy
- zespoły chorobowe:
- encefalopatia związana z zakażeniem HIV (zaburzenia neuropoznawcze związane z HIV)
- zespół wyniszczenia (wyczerpania) spowodowany zakażeniem HIV
Zakażenia wirusowe
- CMV
Infekcja cytomegalowirusem (CMV) przed wprowadzeniem leczenia antyretrowirusowego była jedną z najczęstszych zakażeń oportunistycznych. Choroba zwykle jest następstwem reaktywacji zakażenia latentnego, najczęściej pojawia się przy obniżeniu liczby limfocytów CD4+ <50 komórek/μl. W przebiegu reaktywacji zakażenia latentnego może dochodzić do ciężkiej manifestacji narządowej.
Cytomegalowirusowe zapalenie siatkówki objawia się stopniowym, a rzadziej o szybkim przebiegu, upośledzeniem widzenia, mogą pojawiać się mroczki. Nieleczona choroba prowadzi do utraty wzroku. W badaniu dna oka często są obecne wybroczyny okołonaczyniowe oraz złogi włóknika przypominające kłębki waty (tzw. "obraz białego sera z keczupem"), które wyprzedzają objawy utraty wzroku. Zapalenie płuc wywołane przez CMV przebiega podobnie jak inne śródmiąższowe zapalenia płuc, występuje duszność, suchy męczący kaszel. Zakażenie cytomegalowirusem w obrębie przewodu pokarmowego może przebiegać jako zapalenie przełyku z głębokimi owrzodzeniami, objawiające się utrudnionym lub bolesnym połykaniem. Zapalenie jelita cienkiego lub grubego może naśladować nieswoiste zapalenia jelit lub niedokrwienne zapalenie jelita grubego przebiegając gorączką, biegunką, często z domieszką krwi, a przy ciężkim zajęciu może dość do perforacji jelita. Możliwe jest zapalenie dróg żółciowych oraz zapalenie pęcherzyka żółciowego. Ciężką postacią zakażenia CMV jest zapalenie mózgu. Inna postacią zakażenia CMV jest postępująca radikulopatia przebiegająca z osłabieniem kończyn dolnych aż do porażenia wiotkiego oraz zaburzeniem funkcji zwieraczy.
- HSV-1 i HSV-2
Zakażenie wirusem opryszczki pospolitej (HSV) może wywoływać rozległe zmiany w obrębie błon śluzowych oraz skóry. W postaci rozsianej występują uogólnione zmiany skórne z zajęciem narządów wewnętrznych. Ponadto HSV może powodować zapalenie płuc, zapalenie oskrzeli z owrzodzeniami błony śluzowej. HSV wywołuje zapalenie mózgu i opon mózgowo-rdzeniowych o bardzo ciężkim przebiegu.
- VZV
Pierwotne zakażenie wirusem ospy wietrznej i półpaśca cechuje się bardzo ciężkim przebiegiem, często z zapaleniem płuc. Reaktywacja utajonego zakażenia VZV objawia się jako półpasiec.
- JCV i BKV
JC papowa (JCV) i BKV należą do poliomawirusów. Zakażenie JCV jest powszechne, około 80% osób wykazuje obecność przeciwciał przeciw wirusowi. Wirus wykazuje zdolność do przetrwania w stanie uśpienia w nerkach. U chorych w głębokiej immunosupresji z liczbą limfocytów CD4+ poniżej 100 komórek/μl dochodzi do rozwoju postępującej wieloogniskowej leukoencefalopatii (PML). Wirus zakaża oligodendrocyty oraz astrocyty zaburzając produkcję gleju i prowadzi do choroby demielinizacyjnej. W następstwie zajęcia istoty białej pojawiają się objawy ogniskowe oraz zaburzenia świadomości bez gorączki i objawów oponowych. Choroba ostatecznie prowadzi do zgonu chorego. W rezonansie magnetycznym obecne są liczne rozsiane ogniska demielinizacji.
- Koinfekcja HIV i HBV oraz HIV i HCV
Ze względu na podobną drogę transmisji często rozpoznaje się koinfekcję HIV i wirusów hepatotropowych. Koinfekcja trzykrotnie przyspiesza progresję choroby do marskości
Zakażenia bakteryjne
- Zapalenie płuc
Rozpoznanie więcej niż jednego zapalenia płuc w ciągu 12 miesięcy u zakażonych HIV wskazuje na AIDS. Zapalenie płuc u chorych na AIDS wiąże się z cięższym przebiegiem i znacznie wyższą śmiertelnością niż w populacji ogólnej. Często występuje obustronne zapalenie płuc.
- Gruźlica
Gruźlica jest jedną z najczęstszych chorób wskaźnikowych AIDS. Ocenia się, że jedna trzecia chorych na HIV jest zakażona prątkiem gruźlicy. Kluczową rolę w kontroli zakażenia prątkiem gruźlicy pełnią limfocyty CD4+, które wpływają na zatrzymaniu prątków gruźlicy wewnątrz aktywowanych makrofagów tworzących ziarniniaki. U osób immunokompetentnych ostatecznie dochodzi do obumarcia prątków wewnątrz ziarniniaków, jednak wraz ze spadkiem limfocytów CD4+ spada zdolność do utrzymywania prątków wewnątrz makrofagów, co systematycznie zwiększa ryzyko reaktywacji latentnego zakażenia. Jednocześnie samo zakażenie prątkiem gruźlicy pogłębia deficyty immunologiczne związane z zakażeniem HIV.
Gruźlica może wystąpić na każdym etapie klinicznym zakażenia HIV. Obraz kliniczny reaktywacji gruźlicy u chorych zakażonych zmienia się w zależności od liczby limfocytów CD4+. Przy liczbie limfocytów CD4+ >200 komórek/μl obserwuje się typowe zmiany dla gruźlicy w szczytach płuc z tendencją do tworzenia jam, z kolei u chorych z liczbą limfocytów CD4+ <200 komórek/μl, szczególnie <50 komórek/μl, stwierdza się zmiany rozsiane (prosówka) albo zmiany obejmują również środkowe i dolne pola płucne.
Gruźlica pozapłucna dotyczy chorych z liczbą limfocytów CD4+ <200 komórek/μl. Postać pozapłucna może towarzyszyć gruźlicy płuc lub występować niezależnie od zmian w płucach. Najczęstszą postacią jest limfadenopatia trzewna, często z tworzeniem ropni. Innymi postaciami gruźlicy pozapłucnej są gruźlicze zapalenie opłucnej, osierdzia, opon mózgowo-rdzeniowych, zmiany mogą pojawiać się w obrębie skóry, kości, stawów, jelita oraz w innych narządach. Klinicznie choroba manifestuje się pod postacią powiększonych węzłów chłonnych, nacieków zapalnych, ropni, dolegliwości bólowych, stanów podgorączkowych lub gorączki, nocnych potów i wyniszczenia.
- Mykobakteriozy
Do mykobakterioz atypowych o największym znaczeniu klinicznym zalicza się Mycobacterium avium complex (MAC) do których zalicza się Mycobaterium avium i Mycobacterium intracellularae. Stanowią one czynnik etiologiczny 95% zakażeń prątkami niegruźliczymi. Są to organizmy saprofityczne powszechnie występujące w środowisku. Chorują głównie osoby z bardzo ciężkim deficytem immunologicznym z liczbą limfocytów CD4+ <50 komórek/μl. Choroba najczęściej jest wynikiem świeżej infekcji, znacznie rzadziej jest to reaktywacja zakażenia latentnego. Obecnie rzadziej rozpoznaje się postacie uogólnione (septyczne), a częściej ograniczone (narządowe). Postać uogólniona cechuje się gorączką, nocnymi potami, utratą masy ciała, powiększeniem wątroby oraz powiększeniem węzłów chłonnych. Postać płucna objawia się podobnie jak gruźlica. Częściej niż uogólnioną chorobę rozpoznaje się mykobakteriozowe zapalenie węzłów chłonnych. Węzły wykazują tendencję do tworzenia ropni i przetok. Postać zlokalizowana może przebiegać również jako zapalenie płuc oraz zakażenie układu pokarmowego z bólem brzucha, utratą masy ciała, a rzadziej biegunką.
- Biegunka u chorych na AIDS
Przed wprowadzeniem leczenia antyretrowirusowego większość biegunek była spowodowana infekcjami oportunistycznymi. Ze względu na powodowane zaburzenia wchłaniania, niedożywienie i wyniszczenie była istotną przyczyną zwiększonej śmiertelności u chorych na AIDS. Obecnie ze względu na skuteczność leczenia i związane z nim działania niepożądane nastąpiło znaczne przesunięcie w kierunku przyczyn niezakaźnych. W zależności od populacji, definicji biegunki i metodologii badania ocenia się, że problem dotyczy około 30–55% chorych na AIDS.
Układ pokarmowy zawiera tkankę limfatyczną związaną z błonami śluzowymi przewodu pokarmowego (GALT), który stanowi największy zbiór tkanki limfoidalnej u człowieka, pełni ona rolę w odpowiedzi na liczne antygeny dostarczane z pożywieniem. Z powodu większej ekspresji receptora CCR5 oraz stałej fizjologicznej aktywacji układu immunologicznego w obrębie GALT dochodzi do wzmożonej replikacji wirusa HIV, co prowadzi do szybszego i bardziej zaznaczonego niż w obszarach niedoboru limfocytów CD4+. Niedobór limfocytów CD4+ może się lokalnie utrzymywać nawet pomimo skutecznej terapii antyretrowirusowej i powrotu prawidłowej liczby limfocytów CD4+ na obwodzie.
Do najważniejszych bakteryjnych czynników etiologicznych biegunek należy Salmonella sp., Shigella sp., Campylobacter jejuni i Clostridium difficile, Escherichia coli oraz Mycobacterium avium complex (MAC). Antybiotykoterapia o szerokim spektrum sprzyja biegunce o etiologii Clostridium difficile. Jednym z najczęstszych wirusowych przyczyn biegunki u chorych na AIDS jest cytomegalia, ale biegunka może być związana również z adenowirusami, rotawirusami, norowirusami, koronawirusami czy wirusem opryszczki pospolitej. Cryptosporidium parvum powodujące kryptosporydiozę, mikrosporydia, Isospora belli, Cyclospora, Giardia lamblia, Toxoplasma gondii są najczęstszymi pierwotniakami powodującymi biegunkę u chorych na AIDS.
Do najważniejszych przyczyn niezakaźnych biegunki u chorych na AIDS jest enteropatia związana z HIV oraz działania niepożądane leków antyretrowirusowych. Enteropatia związana z HIV może pojawić się na każdym etapie zakażenia HIV, zarówno w fazie ostrej, jak i już w rozwiniętym zespole nabytego niedoboru odporności. W przebiegu enteropatii związanej z HIV obserwuje się zanik mikrokosmków oraz przerost krypt jelitowych. Najprawdopodobniej czynnikiem sprawczym enteropatii jest wpływ wirusa na strukturę i funkcję enterocytów oraz zaburzenie ich różnicowania się, a także lokalna aktywacja układu immunologicznego skutkująca produkcją cytokin prozapalnych, zapaleniem błony śluzowej oraz jej uszkodzeniem. W rezultacie dochodzi do zwiększenia przepuszczalności błony śluzowej jelita, biegunki i zaburzeń wchłania. Biegunka może być działaniem niepożądanym leczenia antyretrowirusowego, HAART może być przyczyną nawet 20% biegunek u chorych z AIDS. Największe ryzyko biegunki niosą ze sobą inhibitory proteazy.
Zakażenia pasożytnicze
- Toksoplazmoza
Toksoplazmoza jest chorobą pasożytniczą wywoływaną przez Toxoplasma gondii. U chorych z rozwiniętym AIDS toksoplazmoza zwykle jest następstwem reaktywacji zakażenia latentnego, zwykle przy liczbie limfocytów CD4+ <50 komórek/μl. Zajęcie ośrodkowego układu nerwowego może przebiegać jako ropień mózgu lub zapalenie mózgu. Wywoływane objawy zależą od lokalizacji zmian, a choroba może przebiegać skąpoobjawowo, wywołać zaburzenia psychiczne, napady drgawek, zaburzenia świadomości, zaburzenia koordynacji, objawy móżdżkowe i wypadnięcie funkcji nerwów czaszkowych lub inne objawy ogniskowe. W przebiegu reaktywacji toksoplazmozy może dojść do toksoplazomowego zapalenia płuc, które jest obarczone bardzo wysoką śmiertelnością. Zapalenie siatkówki i naczyniówki objawia się bólem oka oraz utratą ostrości widzenia. Rzadziej rozpoznaje się zapalenie przewodu pokarmowego, zapalenie wątroby, zapalenie mięśnia sercowego oraz postać rozsianą.
- Kryptosporydioza
Kryptosporydioza jest chorobą pasożytniczą wywołaną przez pierwotniaki Cryptosporidium parvum i Cryptosporidium hominis. Do zakażenia dochodzi na drodze fekalno-oralnej lub poprzez inhalację oocysty. U osób immunokompetentnych w wyniku zakażenia pojawia się samoograniczająca się biegunka. U osób liczbą limfocytów CD4+ <100–150 komórek/μl dochodzi do rozwoju przewlekłej biegunki z wodnistymi stolcami, odwodnieniem i utratą masy ciała. Możliwe jest zajęcie dróg żółciowych i pęcherzyka żółciowego oraz układu oddechowego.
- Mikrosporydioza
Mikrosporydioza jest wywołana przez obligatoryjne wewnątrzkomórkowe pasożyty mikrosporydie. Najczęściej przebiega pod postacią przewlekłej biegunki z zaburzeniem wchłaniania i niedożywieniem. Jednak możliwy jest rozsiew mikrosporydii i zajęcie dowolnego organu. Opisywano zapalenie mózgu, zapalenie rogówki i spojówek, zapalenie zatok, zapalenie płuc, zapalenie mięśnia sercowego, zapalenie otrzewnej, zapalenie nerek i zapalenie wątroby wywoływane przez mikrosporydie.
Zakażenia grzybicze
- Pneumocystis jiroveci
Pneumocystoza jest śródmiąższowym zapaleniem płuc spowodowanym przez Pneumocystis jiroveci. Przed wprowadzeniem HAART i profilaktyki antybiotykowej była to jedna z najczęstszych chorób wskaźnikowych AIDS. Pneumocystoza zwykle pojawia przy spadku liczby limfocytów CD4+ poniżej 100 komórek/μl. Pneumocystoza objawia się powoli narastającą dusznością, suchym kaszlem, gorączką, nocnymi potami. Choroba może doprowadzić do niewydolności oddechowej. W zdjęciu rentgenowskim klatki piersiowej widoczne są zmiany śródmiąższowe o obrazie „mlecznej szyby” najbardziej nasilone w obrębie dolnych płatów lub w kształcie „skrzydeł motyla”. W gazometrii obecna jest hipoksemia.
- Kandydoza
Candida albicans, a rzadziej Candida tropicalis, Candida glabrata, Candida krusei, może powodować zakażenia skóry i błon śluzowych, ale także układowe zakażenia grzybicze. Obraz zakażeń zmienia się wraz z głębokością niedoborów immunologicznych. Nawracająca kandydoza pochwy może występować również przy prawidłowej liczby limfocytów CD4+, kandydoza jamy ustnej zwykle występuje nieco później w przebiegu zakażenia HIV. Kandydoza pochwy objawia się świądem, pieczeniem, podrażnieniem okolicy pochwy oraz sromu oraz obecnością upławów. Kandydoza jamy ustnej objawia się bólem w jamie ustnej, szczególnie podczas połykania oraz obecnością widocznych białych zmian grzybiczych, które można oddzielić od błony śluzowej. Kandydoza przełyku dotyczy chorych ze znacznie obniżoną liczbą limfocytów CD4+. Zwykle jest następstwem postępu kandydozy jamy ustnej i gardła, manifestuje się bólem podczas połykania oraz zaburzeniami połykania, czasem występuje ból lub uczucie ucisku w klatce piersiowej. Kandydoza tchawicy, oskrzeli i płuc jest bardzo późną manifestacją AIDS, zwykle jest częścią postaci rozsianej kandydozy. Może być następstwem progresji kandydozy jamy ustnej lub wynikiem rozsiewu drogą krwionośną. W postaci rozsianej może dochodzić do zajęcia jednego lub kilku narządów wewnętrznych z tworzeniem mikroropni.
- Kryptokokoza
Kryptokokoza jest to grzybica wywołana przez Cryptococcus neoformans, zakażenia grzybem Cryptococcus zwykle dotyczą osób z niedoborem odporności komórkowej. Najczęściej przebiegają jako zapalenie opon mózgowo-rdzeniowych lub zapalenie płuc. Kryptokokoza płuc może przebiegać jako płatowe zapalenie płuc lub śródmiąższowe zapalenie płuc. Kryptokokowe zapalenie opon mózgowo-rdzeniowych może objawiać się gorączką, nudnościami, wymiotami i objawami ogniskowymi, w tym drgawkami, porażeniem nerwów czaszkowych i zaburzeniami widzenia. U chorych z HIV kryptokokowe zapalenie opon mózgowo-rdzeniowych zwykle dotyczy chorych z bardzo ciężkim obniżeniem liczbie limfocytów CD4+ poniżej 50 komórek/μl. Zmiany skórne w przebiegu kryptokokozy przyjmują formę guzków, grudek lub pęcherzyków zlokalizowanych na twarzy, szyi i owłosionej skóry głowy.
Nowotwory
Do nowotworów definiujących AIDS należy mięsak Kaposiego, niektóre chłoniaki nieziarnicze oraz inwazyjny rak szyjki macicy. W AIDS obserwuje się również zwiększenie ryzyka zachorowania na liczne inne nowotwory złośliwe, w tym raka odbytu, nowotworów głowy i szyi, chłoniaka Hodgkina, raka wątrobowokomórkowego czy raka płuca, których rozpoznanie nie upoważnia do rozpoznania AIDS. W związku z prowadzeniem HAART zaobserwowano zmniejszenie liczby nowych przypadków nowotworów definiujących AIDS, jednak z różnych powodów, głównie wydłużonego przeżycia chorych, nie stwierdzono istotnego spadku liczby przypadków nowotworów niedefiniujących AIDS.
- Mięsak Kaposiego
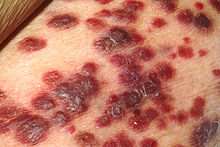
Mięsak Kaposiego jest mięsakiem tkanek miękkich pochodzenia naczyniowego zaliczany do nowotworów o granicznej złośliwości rzadko przerzutujących. Proces karcynogenezy nowotworu jest ściśle powiązany z zakażeniem KSHV (HHV-8). Szacuje, że AIDS 20 000-krotnie zwiększa ryzyko zachorowania na mięsaka Kaposiego. Ryzyko rozwoju mięsaka Kaposiego jest wyższe u homoseksualnych mężczyzn. Zmiany skórne początkowo przybierają formę licznych, drobnych, różowych, fioletowych, czerwononiebieskich, czerwonobrunatnych ostro ograniczonych, niebolesnych plamek, które przekształcają się w grudki, guzki lub blaszki. Zmiany mogą występować w dowolnej lokalizacji skóry, błon śluzowych oraz węzłów chłonnych i narządów wewnętrznych, przede wszystkim w płucach, przewodzie pokarmowym, wątrobie i śledzionie.
- Chłoniaki nieziarnicze
Przed wprowadzeniem HAART chłoniaki u zakażonych HIV występowały ponad stukrotnie częściej niż w populacji ogólnej i dotyczyły 2–10% chorych na HIV. Wprowadzenie skutecznego leczenia antyretrowirusowego znacząco zmniejszyło ryzyko rozwoju chłoniaków nieziarniczych. U chorych z HIV chłoniaki zwykle są rozpoznawane w bardziej zaawansowanych stadiach, u chorych występują objawy ogólne, występuje tendencja do występowania chłoniaka poza narządami limfatycznymi i węzłami chłonnymi z zajęciem szpiku, wątroby, przewodu pokarmowego i centralnego układu nerwowego.
Chłoniak rozlany z dużych komórek B (DLBCL) występuje zarówno u osób zakażonych HIV, jak i u niezakażonych tym wirusem. Na podstawie morfologii są dzielone na centroblastyczne i immunoblastyczne. Oba podtypy występują z podobną częstością u chorych na AIDS. Podtyp immunoblastyczny jest w znacznym stopniu związany z zakażeniem EBV (80–90%), zwykle pojawia się u chorych z głębokim niedoborem odporności w zaawansowanym AIDS. Podtyp centroblastyczny może występować również bez związku z AIDS, jest w znacznie mniejszym stopniu związany z EBV (30–40%). Pierwotny chłoniak ośrodkowego układu nerwowego jest podtypem chłoniaka rozlanego z dużych komórek B, który jest podobny do typu immunoblastycznego.
Chłoniak Burkitta może występować bez związku z zakażeniem HIV, a u zakażonych HIV może pojawić się przy liczbie limfocytów CD4+ powyżej 200 komórek/μl, a więc nie spełniającej laboratoryjnej definicji AIDS. Może stanowić 30–40% wszystkich chłoniaków nieziarniczych u zakażonych HIV. Klinicznie chłoniak Burkitta charakteryzuje się bardzo agresywnym przebiegiem, z szybkim czasem podwojenia masy guza i gwałtownym rozwojem objawów klinicznych. W przebiegu choroby dochodzi do zajęcia węzłów chłonnych, szpiku kostnego i lokalizacji pozawęzłowych (narządów pozalimfatycznych), często w obrębie jamy brzusznej.
Pierwotny chłoniak jam surowiczych występuje niemal wyłącznie u chorych na AIDS. Chłoniak stanowi około 5% chłoniaków nieziarniczych u zakażonych HIV. Nowotwór etiologicznie jest ściśle związany z wirusem KSHV (HHV-8). Klinicznie objawia się jako wysięk w jamie opłucnej, otrzewnej czy osierdziu, zwykle bez utworzenia jawnego guza. W jednej trzeciej przypadków stwierdza się rozsiew poza błony i jamy surowicze.
Chłoniak plazmablastyczny jest odrębnym podtypem chłoniaka rozlanego z dużych komórek B, najczęściej występującego w zakresie jamy ustnej i szczęki, cechuje się szybkim i agresywnym przebiegiem.
- Rak szyjki macicy
Kobiety zakażone wirusem HIV mają 1,5–8-krotnie zwiększone ryzyko rozwoju raka szyjki macicy. Nowotwór jest przyczynowo związany z zakażeniem wirusami HPV 16 i 18. U kobiet zakażonych HIV z liczbą limfocytów CD4+ <200 komórek/μl częściej niż w populacji ogólnej występują onkogenne typy HPV, stwierdza się wyższą wiremię, a ponadto częściej stwierdza się koinfekcję różnych podtypów wirusa HPV. Początkowo rak szyjki macicy może przebiegać bezobjawowo, następnie pojawiają się nieprawidłowe krwawienia z dróg rodnych i ból w obrębie miednicy małej.
- Nowotwory złośliwe niedefiniujące AIDS
U chorych zakażonych HIV obserwuje się 2,5–3,5-krotne zwiększenie ryzyko zachorowania na raka płuca. Wyższe ryzyko zachorowania jest obserwowane we wszystkich najważniejszych typach histologicznych raka płuca, a ryzyko rozwoju choroby u zakażonych HIV nie zmieniło wprowadzenie HAART. Zwiększone ryzyko zachorowania na raka płuc może być związane z większym rozpowszechnieniem palenia tytoniu wśród zakażonych HIV niż w populacji ogólnej. Z drugiej strony zwiększone ryzyko zachorowania na raka płuc nie może być wytłumaczone wyłącznie zwiększoną częstością palenia tytoniu. Prawdopodobnie przewlekły stan zapalny, nawracające infekcje i upośledzenie odporności działają synergistycznie z paleniem tytoniu promując rozwój nowotworu.
U osób zakażonych HIV od sześciu do siedmiokrotnie częściej rozpoznaje się raka wątrobowokomórkowego niż w populacji ogólnej. Jest to związane z częstszym zakażeniem wirusami hepatropowymi HCV i HBV wykazujących działanie karcynogenne w patogenezie raka wątrobowokomórkowego. Koinfekcja HCV i HBV z wirusem HIV jest związana z podobną drogą transmisji tych wirusów. Ocenia się, że w Europie Zachodniej i Ameryce Północnej nawet u 25% chorych na HIV współwystępuje koinfekcja HCV. Nie ma dowodu na bezpośredni wpływ HIV na karcynogenezę raka wątrobowokomórkowego. Jednak wirus znacznie przyspiesza progresję przewlekłego zapalenia wątroby do marskości i ostatecznie do raka.
Chorzy na HIV dziesięciokrotnie częściej chorują na chłoniaka Hodgkina. HAART nie zmniejszyło zapadalności na chłoniaka Hodgkina u zakażonych HIV, a wręcz zaobserwowano wzrost liczby zachorowań. Prawdopodobnie wynika to ze zwiększenia liczby limfocytów CD4+, co pozwala odtworzyć mikrośrodowisko komórkowe otaczające komórki Reed-Sternberga i umożliwić manifestację choroby.
Rak odbytu w populacji ogólnej jest stosunkowo rzadkim nowotworem, podobnie jak rak szyjki macicy jest etiologicznie powiązany z zakażeniem HPV, a także z paleniem tytoniu oraz stosunkami analnymi biernymi. U zakażonych HIV stwierdzono dwudziestopięciokrotnie zwiększone ryzyko raka odbytu, a u homoseksulanych mężczyzn (MSM) zakażonych HIV aż osiemdziesięciokrotne zwiększone ryzyko zachorowania na raka odbytu. Większa częstość występowania raka odbytu u zakażonych HIV jest wiązana z częstszym zakażeniem HPV, co jest związane z częstszym występowaniem ryzykownych zachowań seksualnych u zakażonych HIV oraz prawdopodobnie z immunosupresją, która może wpływać na rozwój oraz bardziej agresywny przebieg tego raka.
Nowotwory głowy i szyi są to głównie nowotwory płaskonabłonkowe etiologicznie związane z paleniem tytoniu, spożywaniem alkoholu oraz zakażeniem HPV. Ocenia się, że zakażeni wirusem HIV mają od dwu do czterokrotnie zwiększone ryzyko zachorowania na nowotwory głowy i szyi.
Zanotowano również zwiększone ryzyko rozwoju czerniaka, nowotworów skóry, raka nerki oraz białaczek.
Zespoły chorobowe
- Zespół wyniszczenia spowodowany zakażeniem HIV
W konsekwencji zakażenia wirusem HIV dochodzi do zaburzenia przemiany materii i odżywania, które ostatecznie mogą doprowadzić do zespołu wyniszczenia (ang. AIDS wasting syndrome). Zespół wyniszczenia jest definiowany jako niezamierzona utrata ponad 10% masy ciała z towarzyszącą przewlekłą biegunką (przynajmniej dwa luźne stolce dziennie przez ponad 30 dni) albo udokumentowaną gorączką trwającą ponad 30 dni z przewlekłym osłabieniem. Jednocześnie nie stwierdza się innego stanu, który mógłby wyjaśniać takie objawy. Zespół jest powodem przyspieszonej progresji choroby i zwiększonej śmiertelności chorych oraz znacznego pogorszenia jakości ich życia. U przyczyn zespołu leżą zaburzenia łaknienia, zaburzenia wchłaniania, zmniejszona kaloryczność pożywienia, zwiększone zapotrzebowanie metaboliczne oraz zaburzenia hormonalne.
- Zaburzenia neuropoznawcze związane z HIV
W przebiegu zaawansowanego zakażenia, niezależnie od obecności zakażeń oportunistycznych, dochodzi do rozwoju spektrum zaburzeń poznawczych, motorycznych i zachowania o różnym stopniu nasilenia określanych jako zaburzenia neuropoznawcze związane z HIV (HIV-Associated Neurocognitive Disorder, HAND). Wyróżnia się trzy zespoły chorobowe wchodzące w skład zaburzeń poznawczych związanych z HIV – bezobjawowe zaburzenia neuropoznawcze związane z HIV, łagodne zaburzenia neuropoznawcze związane z HIV i HIV-demencja kompleks. Częstość zaburzeń poznawczych u zakażonych HIV nie spada, choć wprowadzenie HAART doprowadziło do spadku częstości występowania jego najcięższych form. Patogeneza HAND raczej nie jest związana z bezpośrednią infekcją neuronów, a pobudzenia mikrogleju związanej z odpowiedzią zapalną na wirusa.
HIV-demencja kompleks pojawia się w zaawansowanej chorobie, prowadzi od umiarkowanych do ciężkich zaburzeń poznawczych z upośledzeniem pamięci, spadkiem zdolności do koncentracji, spowolnieniem i zubożeniem myślenia, abulią, spowolnieniem motorycznym, zaburzeniami chodu i różnymi zaburzeniami zachowania. Zespół prowadzi do śmierci chorego. Przed wprowadzeniem HAART HIV-demencja kompleks była to najczęstszą formą zaburzeń poznawczych związanych z HIV, ale obecnie jego zapadalność spada.
Łagodne zaburzenia neuropoznawcze związane z HIV i bezobjawowe zaburzenia neuropoznawcze związane z HIV są najczęstszymi formami HAND. Łagodne zaburzenia neuropoznawcze związane z HIV cechują się występowaniem łagodnych do umiarkowanych deficytów poznawczych w przynajmniej dwóch obszarach poznawczych zaburzających codzienne funkcjonowanie. Bezobjawowe zaburzenia neuropoznawcze związane z HIV charakteryzują się obecnością lekkich deficytów poznawczych w przynajmniej dwóch obszarach poznawczych, które nie zaburzają codziennego funkcjonowania.
Diagnostyka
Diagnostyka przesiewowa zakażenia wirusem HIV jest oparta o badania serologiczne wykrywające przeciwciała powstałe w konsekwencji odpowiedzi immunologicznej skierowanej przeciw HIV, które są wykrywane za pomocą metod immunoenzymatycznych. W niektórych badaniach oznacza się również swoiste dla wirusa HIV antygeny, co zwiększa czułość diagnostyczną tych badań. Stwierdzenie dodatniego wyniku w testach przesiewowych wymaga weryfikacji w bardziej swoistych badaniach potwierdzenia, w których wykorzystuje się metodę western blot, a rzadziej LIA (line immunoassay). Rozpoznanie zakażenia wirusa nie jest możliwe w okresie inkubacji, czyli przed upływem 7 dni od zakażenia, po tym okresie we krwi pojawia się antygen p24 oraz RNA wirusa, które można wykryć za pomocą odpowiednich badań. Po 3–12 tygodniach od zakażenia pojawiają się swoiste przeciwciała anty-HIV, choć możliwa jest późniejsza serokonwersja. Diagnostyka zakażenia HIV może być przeprowadzona anonimowo. Po uzyskaniu rozpoznania zakażenia HIV diagnostykę poszerza się o badania oceniające wyjściowe zaawansowanie choroby, w tym o badanie liczby limfocytów CD4+, poziomu wiremii i oporności na leki. Oznaczenie poziomu wiremii i liczby limfocytów CD4+ ma znaczenie w monitorowaniu skuteczności leczenia.
Badania przesiewowe
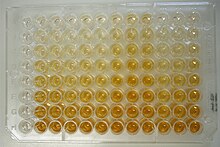
Badania immunoenzymatyczne (EIA) wykrywają przeciwciała anty-HIV wytwarzane w wyniku odpowiedzi immunologicznej przeciw wirusowi HIV. Historycznie testy pierwszej generacji opierały się o wykorzystanie lizatów antygenów wirusa. Surowica zakażonego HIV zawierającą przeciwciała anty-HIV jest dodawana do przymocowanych z podłożem antygenów wirusowych uzyskanych z lizatu hodowli wirusa HIV. Po związaniu swoistych przeciwciał z antygenami wirusa przytwierdzonych do podłoża i przepłukaniu próbki usuwa się inne przeciwciała niż te swoiste dla wirusa HIV. W kolejnym etapie badania dodawane są przeciwciała zwierzęce koniugowane z enzymem wiążące się z badanymi przeciwciałami anty-HIV. Enzym katalizuje barwną reakcję, która może być mierzona w spektofotometrze. W testach immunoenzymatycznych II generacji zamiast lizatu jako źródła antygenów wirusa zastosowano antygeny pozyskiwane metodą rekombinacji, co zwiększyło czułość badania.
Obecnie zastosowanie w diagnostyce znajdują testy trzeciej i czwartej generacji. W testach trzeciej generacji stosuje się rekombinowane antygeny wirusa HIV oraz dodatkowo antygeny znakowane enzymatycznie (sandwich antigen). Z kolei testy czwartej generacji, poza wykrywaniem przeciwciał anty-HIV, pozwalają na potwierdzenie obecności antygenu p24, co umożliwia na rozpoznanie zakażenia na wcześniejszym etapie zakażenia i znacząco skraca okres "okna diagnostycznego". Przekłada się to na mniejszą liczbę wyników fałszywie ujemnych. Testy IV generacji wykrywające antygen p24 są przydatne w rozpoznawaniu zakażenia HIV w zaawansowanym stadium klinicznym, kiedy wiremia jest bardzo wysoka, a ilość przeciwciał anty-HIV może być już nieoznaczalna.
Testy immunoenzymatyczne wykazują bardzo wysoką czułość i wysoką swoistość, jednak żadna metoda nie wyklucza wyniku fałszywie ujemnego lub fałszywie dodatniego. Ze względu na wykrywanie w testach IV generacji zakażenia HIV przed serokonwersją (wytworzeniem przeciwciał) cechują się one większą czułością niż testy III generacji. Swoistość testów IV generacji jest niższa od testów III generacji. Szacuje się, że czułość testów III generacji w wykrywaniu HIV po około 3 miesiącach od zakażenia wynosi 99,8–100%, a testów IV generacji 99,76–100%. Swoistość testów III generacji jest oceniana na 99,13–100%, a testów IV generacji na 99,5–100%.
Ograniczeniem testów opartych na wykrywaniu przeciwciał oraz antygenów wirusa jest okienko diagnostyczne. We wczesnym etapie infekcji HIV pomimo replikacji wirusa jeszcze nie doszło wytworzenia przeciwciał anty-HIV, przez co metody oparte o ich wykrywanie w tym okresie nie pozwalają na rozpoznanie zakażenia. U większości chorych w ciągu 3 tygodni od zakażenia pojawiają się przeciwciała IgM, których szczyt stężenia przypada na 4 i 5 tydzień, jednak przeciwciała IgM nie są wykrywalne u wszystkich chorych. Po 3–4 tygodniach od zakażenia pojawiają się przeciwciała IgG. Ich miano osiąga szczyt w ciągu 10–12 tygodni. Niemal u wszystkich chorych w ciągu 1–2 miesięcy powstają przeciwciała wykrywalne za pomocą rutynowych, komercyjnych testów immunoenzymatycznych, ale u niewielkiego odsetka chorych serokonwersja zachodzi później w ciągu 6 miesięcy od zakażenia. Przyjmuje się, że testy III generacji pozwalają na wykrycie przeciwciał anty-HIV po 4–12 tygodniach od zakażenia, a testy IV generacji na rozpoznanie obecności antygenu p24 po 2–3 tygodniach od zakażenia i wykrycie przeciwciał anty-HIV po 4–12 tygodniach od zakażenia.
W okresie okienka serologicznego zakażenie pozwalają rozpoznać testy immunoenzymatyczne IV generacji wykrywające poza obecnością przeciwciał również obecność antygenu p24. Antygen p24 można wykryć po 11–13 dni od infekcji wirusem HIV, nieco później niż RNA wirusa. Zatem w okresie inkubacji, przed pojawieniem się antygenu p24 test IV generacji da ujemny wynik. Antygen p24 pozostaje wykrywalny do miesiąca od zakażenia. Ponadto w starszych wersjach testów IV generacji możliwe jest rzadkie zjawisko "drugiego okienka diagnostycznego" związanego ze spadkiem stężenia antygenu p24 tuż przez pojawieniem się przeciwciał anty-HIV.
W przypadku stwierdzenia dodatniego (reaktywnego) wyniku na obecność przeciwciał anty-HIV w badanej próbce krwi, konieczne jest powtórzenie badania z pobraniem drugiej próbki krwi. Stwierdzenie w dwóch niezależnych próbówkach wyniku dodatniego w kierunku przeciwciał anty-HIV sugeruje obecność przeciwciał anty-HIV i wymaga dalszej diagnostyki. Ze względu na możliwość niespecyficznej reaktywności dodatni wynik bezwzględnie wymaga weryfikacji w badaniach potwierdzających. Przed uzyskaniem dodatniego wyniku w teście potwierdzenia nie można rozpoznać zakażenia wirusem HIV. Fałszywie dodatni wynik testu przesiewowego może być związany z nieswoistą aktywacją układu immunologicznego w przebiegu ostrych infekcji, chorób autoimmunologicznych, nowotworu złośliwego, niedawnego szczepienia, ciąży, stanu po przeszczepie oraz przetoczeniu krwi. Ujemny wynik testu przesiewowego nie wymaga weryfikacji, chyba że istnieje podejrzenie wykonania badania w okresie "okienka serologicznego", wówczas w uzasadnionych przypadkach wykonuje się ponowne badanie po 3 miesiącach.
Badania potwierdzające zakażenie HIV
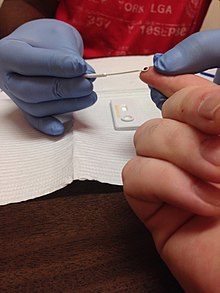
Dodatni wynik testu przesiewowego, ze względu na ryzyko wyniku fałszywie dodatniego, wymaga potwierdzenia w badaniach potwierdzających, w których najczęściej wykorzystuje się badanie western blot, a rzadziej LIA (line immunoassay). Testy potwierdzenia nie powinny być stosowane w diagnostyce zakażenia HIV jako pierwsze lub jako jedyne. Badanie cechuje się wysoką ceną i dość trudną interpretacją, stosunkowo często uzyskuje się niejednoznaczne wyniki, które dodatkowo zwiększają koszt badania.
W metodzie western blot do rozdzielonych za pomocą elektroforezy i unieruchomionych w podłożu nitrocelulozowym białek wirusa HIV dodaje się badaną surowicę. Jeśli badana surowica zawiera odpowiednie przeciwciała anty-HIV to ulegną one związaniu z rozdzielonymi białkami wirusa HIV. W kolejnym etapie badania w celu wizualizacji obecności związanych przeciwciał dodaje się kolejne przeciwciała wiążące się z badanymi przeciwciałami anty-HIV, dodane przeciwciała zawierają sprzężony enzym pozwalający na powstanie barwnej reakcji widocznej jako pasek. W metodzie wykorzystuje się produkty genów env (gp41, gp120, gp160), gag (p17, p24/25, p55) i pol (p34, p40, p52, p68). Wynik badania może być dodatni, ujemny lub niejednoznaczny (nieokreślony). Wynik niejednoznaczny może odzwierciedlać reakcję graniczną albo niespecyficzną. Za wynik dodatni uważa się obecność przeciwciał widocznych jako prążki przeciw antygenom dwóch różnych grup białek env, gag i pol. W kryteriach WHO do rozpoznania choroby koniecznym warunkiem jest stwierdzenie obecności przeciwciał przeciw białkom osłonki (gp41, gp120, gp160). Z kolei w kryteriach CDC za wynik dodatni uznaje się stwierdzenie obecności przeciwciał przeciw p24, gp41, gp120 lub gp160.
W wyjątkowych sytuacjach, jak podejrzenie ostrej choroby retrowirusowej, wczesnego etapu zakażenia HIV, porodu czy konieczność pilnego włączenia leczenia antyretrowirusowego z powodu AIDS, rozpoznanie zakażenia może być postawione na podstawie stwierdzenia obecności materiału genetycznego wirusa (RNA) we krwi, przy czym zaleca się potwierdzenie zakażenia HIV za pomocą testów wykrywających przeciwciała w późniejszym okresie.
Schemat diagnostyczny
Ujemny wynik w kierunku HIV w badaniu przesiewowym nie wymaga potwierdzenia. W przypadku podejrzenia wykonania badania w okresie okienka serologicznego można oznaczyć antygen p24, a następnie powtórzyć badania po przynajmniej 2 tygodniach. Stwierdzenie w dwóch niezależnych próbkach wyniku dodatniego wymaga wykonania testu potwierdzenia, jakim jest western blot. Dodatnie wyniki immunoenzymatycznych testów przesiewowych z dwóch próbek (optymalnie pobranych z dwóch osobnych pobrań) oraz dodatniego wyniku testu potwierdzenia western blot lub LIA pobranego z osobnej próbki uzasadnia rozpoznanie zakażenia HIV. Podobnie do rozpoznania HIV upoważnia stwierdzenie obecności w dwóch próbkach RNA wirusa HIV.
Stwierdzenie dwóch dodatnich wyników badań przesiewowych przy ujemnych testach potwierdzenia może wiązać się z fałszywie dodatnim wynikiem mniej swoistego testu przesiewowego, ale także z obecnością antygenu p24 i obecnością przeciwciał w klasie IgM, które mogę być wykrywane w testach przesiewowych, ale nie są wykrywane w testach potwierdzenia. W przypadku rozbieżnych wyników testów przesiewowych konieczne jest powtórzenie badania.
Szybkie testy anty-HIV
Szybkie testy anty-HIV są metodami opartymi o aglutynację cząsteczkową, immunodot, immunofiltrację, immunochromatografię i pozwalają one na uzyskanie wyniku w ciągu 15–30 minut.
Zwykle materiałem jest krew włośniczkowa pobraną z palca lub płatka ucha. W niektórych testach wykorzystuje się suchą kroplę krwi, ślinę lub mocz. Testy oparte o suchą kroplę krwi nie wymagają filtracji krwi, a wyschnięta krew nie stanowi istotnego materiału zakaźnego. Testy bazujące na suchej kropli krwi znajdują zastosowanie jako metoda badań przesiewowych w krajach rozwijających się o ograniczonej dostępności do odpowiednich laboratoriów i właściwych warunków transportowych próbek.
Szybkie testy anty-HIV charakteryzują się mniejszą czułością diagnostyczną niż konwencjonalne immunoenzymatyczne testy przesiewowe, a więc wynik ujemny takiego szybkiego testu ma mniejszą ujemną wartość predykcyjną. Wynik dodatni wymaga potwierdzenia za pomocą testów immunoenzymatycznych a następnie testów potwierdzenia. Szybkie testy anty-HIV mają znaczenie w diagnostyce przesiewowej zakażenia wirusem HIV w krajach rozwijających się, a w krajach rozwiniętych w sytuacjach wymagających szybkiego uzyskania wyniku, szczególnie w przypadku ekspozycji zawodowej, wysokiego ryzyka nieodebrania wyniku oraz badania u kobiet rodzących, które nie miały wykonywanego badania w kierunku HIV podczas ciąży.
Oznaczanie liczby limfocytów CD4+
Oznaczanie liczby limfocytów CD4+ w proporcji do limfocytów CD8+ służy do monitorowania czynności układu immunologicznego. Jest przydatnym wskaźnikiem do oceny skuteczności leczenia antyretrowirusowego. Spadek liczby limfocytów CD4+ sugeruje progresję choroby, a z kolei wzrost liczby limfocytów CD4+ przemawia za skutecznością leczenia.
Prawidłowa liczba limfocytów CD4+ u dorosłych waha się od 500 do 1500 komórek/μl. Wyjściowa liczba limfocytów CD4+ jest oznaczana każdego chorego z rozpoznanym zakażeniem HIV. Następnie w celu monitorowania leczenia początkowo oznacza się ich liczbę co 2–3 miesiące, choć przy liczbie limfocytów CD4+ >500 komórek/μl oznaczenia można wykonywać co 6 miesięcy. W interpretacji wyniku liczby limfocytów CD4+ pod uwagę bierze się metodę diagnostyczną, wahania związane z innymi infekcjami oraz wahania sezonowe.
Oznaczanie poziomu wiremii
Badania genetyczne w diagnostyce zakażenia HIV wykrywają materiał genetyczny wirusa HIV RNA lub komplementarny DNA HIV. Standardem diagnostycznym jest reakcja łańcuchowa polimerazy, do której startery i sondy zostały uzyskane na podstawie genonu HIV.
Jakościowe oznaczenie obecności HIV RNA pozwala na stwierdzenie obecności materiału genetycznego wirusa i potwierdzenie zakażenia HIV. Metoda pozwala na wykrycie wiremii HIV na poziomie 40–50 kopii w mililitrze. Jakościowe oznaczenie wiremii jest wykorzystywane w badaniu wybranych chorych po ekspozycji z podejrzeniem wczesnej fazy zakażenia przed serokonwersją, u chorych z podejrzeniem późnej serokonwersji oraz u chorych z dodatnim testem przesiewowym i ujemnym testem western blot. Badanie jest przydatne w rozpoznawaniu zakażenia HIV u noworodków i niemowląt matek nosicielek wirusa HIV, u których są obecne odmatczyne przeciwciała anty-HIV uniemożliwiające wiarygodną diagnostykę serologiczną. Potwierdzenie zakażenia HIV metodami genetycznych testów jakościowych lub ilościowych jest równoważne testowi western blot.
Ilościowe oznaczenie HIV RNA jest wykonywane za pomocą PCR w czasie rzeczywistym, pozwala na określenie poziomu wiremii, który jest podawany w ilościach kopii w mililitrze. Ilościowo wiremię ocenia się u każdego chorego z rozpoznaniem zakażenia HIV. U leczonych chorych okresowo, około dwa razy do roku, ocenia się poziom wiremii celem oceny skuteczności leczenia. Z kolei u nieleczonych zakażonych HIV również około dwa razy do roku oznacza się poziom wiremii, co pozwala na monitorowanie przebiegu choroby i wybrania odpowiedniego momentu włączenia leczenia. Zaleca się by monitorowanie poziomu wiremii było wykonywane jedną metodą diagnostyczną.
Profilaktyka
Charakterystyka szerzenia się zakażenia HIV wymaga złożonego, wieloaspektowego podejścia do jego profilaktyki. Wirus HIV szerzy się za pośrednictwem kontaktów seksualnych, poprzez kontakt z zakażoną krwią lub drogą wertkalną (z matki na dziecko). Pod względem epidemiologicznym na świecie najważniejszą drogą zakażenia jest droga seksualna, która pośredniczy okołu 80% infekcji. Nie istnieje skuteczna szczepionka przeciw HIV, nie ma też możliwości całkowitego wyleczenia choroby. Podstawowymi metodami profilaktyki jest stosowanie prezerwatyw podczas stosunków seksualnych, ograniczanie liczby partnerów seksualnych, abstynencja seksualna oraz wyłącznie jednorazowe korzystanie ze sprzętu do wstrzykiwań.
Profilaktyka zakażeń HIV za pośrednictwem kontaktów seksualnych
Profilaktyka zakażeń HIV przenoszonych drogą kontaktów seksualnych polega głównie na redukcji ilości niezabezpieczonych kontaktów seksualnych, ograniczaniu ryzykownych zachowań seksualnych oraz promowaniu stosowania prezerwatyw.
W profilaktyce zakażenia HIV kluczowe znaczenie ma unikanie ryzykownych zachowań seksualnych. Zaleca się zmniejszenie liczby partnerów seksualnych, unikanie kontaktów seksualnych bez zabezpieczenia, promowanie stosowania prezerwatyw, unikania korzystania z usług pracowników seksualnych i opóźnianie wieku inicjacji seksualnej. W celu promowania świadomych decyzji dotyczących zachowań seksualnych przeprowadza się kampanie społeczne obejmujące kształtowanie wiedzy dotyczącej ochrony przed zakażeniem HIV, zmiany ryzykownych zachowań seksualnych (mniejsza liczba partnerów seksualnych, bezpieczniejsze praktyki seksualne) oraz promowania używania prezerwatyw. Bardzo ważne jest zachęcanie do wykonywania badań w kierunku HIV, zmniejszanie stygmatyzacji zakażonych oraz ułatwienie dostępu do leczenia zakażenia HIV. Działania mające na celu zmniejszenie liczby zakażeń HIV poprzez wpływ na zachowania muszą być kompleksowe i nie mogą się skupiać wyłącznie na pojedynczych elementach profilaktyki zakażenia. Strategie behawioralne są niezbędne, ale nie są wystarczające do zmniejszania liczby zakażeń HIV.
Stosowanie prezerwatyw znacząco zmniejsza ryzyko zakażenia wirusem HIV. Prezerwatywa stanowi fizyczną barierę uniemożliwiającą przenikanie wydzielin zawierających wirusa. Prezerwatywa wykazuje skuteczność z zapobieganiu zakażeniu HIV wynoszącą około 85%, przy czym w różnych badaniach klinicznych skuteczność waha 60–95%. W badaniu na 342 HIV-seronegatywnych kobietach w stabilnych monogamicznych związkach, których partnerowi byli zakażeni HIV wykazano, że ryzyko zakażenia HIV było sześciokrotnie wyższe gdy prezerwatywy nie były stosowane lub były stosowane nieregularnie. Z kolei w innym badaniu nie zaobserwowano serokonwersji przy każdorazowym stosowaniu prezerwatyw, podczas serokonwersje były obserwowane u par, które prezerwatywy stosowały nieregularnie. Wadą metody jest możliwość pęknięcia czy zsunięcia prezerwatywy, co przy prawidłowym stosowaniu prezerwatywy zdarza się dość rzadko, w przybliżeniu odpowiednio w 2% i 1% przypadków stosowania. Kobieca prezerwatywa, choć wykazuje podobną skuteczność w zapobieganiu chorób wenerycznych co prezerwatywa, to jednak wymaga ściśle poprawnego użytkowania. Spermicydy (środki plemnikobójcze) nie chronią przed zakażeniem HIV.
W ramach działań profilaktycznych zachęca się do wykonywania badań w kierunku HIV. U osób z dodatnim wynikiem w kierunku HIV umożliwia to rozpoczęcie leczenia oraz działań profilaktycznych dla osób zakażonych, a dla osób niezakażonych stanowi okazję do uzyskania informacji dotyczących profilaktyki zakażenia.
Występowanie innych chorób przenoszonych drogą płciową znacząco zwiększa ryzyko zakażenia HIV. Leczenie chorób przenoszonych drogą płciową pozwala zmniejszyć ryzyko transmisji HIV.
Jednym z programów profilaktyki zakażenia HIV jest strategia ABC (Abstinence, Be faithful, use a Condom), których głównymi założeniami jest promocja abstynencji, szczególnie w stosunku do osób młodych (opóźnianie wieku inicjacji seksualnej), promocji stałych związków seksualnych oraz stosowania prezerwatyw. Osoba stosująca tego typu profilaktykę dobiera sobie jedną lub więcej opcji by dostosować ochronę do swoich potrzeb. Strategia ABC jest krytykowana za koncentrację na heteroseksualnej drodze transmisji wirusa, ograniczoną skuteczność w społeczeństwach o ograniczonej pozycji społecznej kobiet, które nie ma możliwości negocjacji bezpiecznego seksu, brakiem strategii wobec osób stosujących dożylnie narkotyki, osób homoseksualnych oraz tendencji do skupiania się na elementach abstynencji i monogamii.
Osoby w wieku 15–24 stanowią prawie połowę wszystkich nowych zakażeń HIV. Profilaktyka zakażenia HIV w tej grupie wiekowej polega na promocji zdrowia seksualnego, promocji opóźniania wieku inicjacji seksualnej, redukcji liczby partnerów seksualnych i częstości ich zmiany oraz stosowania prezerwatyw. Istotna jest edukacja seksualna osób młodych w ramach edukacji szkolnej, która pozwala na kształtowanie bezpiecznych zachować seksualnych oraz na zdobycie wiedzy odnośnie do zakażenia HIV i sposobów jego transmisji. Kompleksowa edukacja seksualna obejmująca w swoim programie nauczanie o środkach antykoncepcyjnych wpływa na ograniczenie ryzykownych zachowań seksualnych, liczby zakażeń HIV i zakażeń przenoszonych drogą płciową. Edukacja seksualna oparta wyłącznie o abstynencję do ślubu nie dostarcza informacji odnośnie do antykoncepcji, w tym stosowaniu prezerwatyw. Programy profilaktyki oparte o abstynencję mają ograniczoną skuteczność w ograniczaniu ryzykownych zachowań seksualnych i opóźnianiu wieku inicjacji seksualnej. W metaanalizie nie potwierdzono skuteczności w zmniejszeniu ryzyku zakażenia HIV. Ponadto są krytykowane za ograniczanie informacji o metodach profilaktyki o udowodnionej skuteczności w zapobieganiu zakażeniu HIV oraz dyskryminacji osób homoseksualnych.
Profilaktyka przedekspozycyjna (PrEP) polega przewlekłym stosowaniu leku lub leków antyretrowirusowych przez osobę niezakażoną wirusem HIV w grupie wysokiego ryzyka przed ekspozycją na HIV w celu zapobiegnięcia zakażenia wirusem HIV. Metoda znajduje zastosowanie w niektórych regionach świata w profilaktyce zakażenia HIV u osób niezakażonych HIV pozostających w związku z osobą zakażoną HIV, u mężczyzn mających kontakty seksualne z mężczyznami (MSM) oraz u innych kluczowych populacji. Stosowanie profilaktyki przedekspozycyjnej pozwala zmniejszyć ryzyko zakażenia HIV w powyższych populacjach. W profilaktyce przedekspozycyjnej stosuje się tenofowir, który może być łączony z emtrycytabiną.
Profilaktyka zakażenia HIV przez skażone igły
Na całym świecie około 13 milionów osób stosuje dożylnie narkotyki i 1,7 miliona z nich jest zakażona HIV. Ocenia się, że dożylne stosowanie narkotyków jest odpowiedzialne za około 10% zakażeń na świecie i za jedną trzecią przypadków nowych zakażeń HIV w Afryce. W niektórych częściach świata jest to najważniejszą przyczyną zakażeń HIV.
W ramach działań profilaktycznych dedykowanych tej grupie chorych stosuje się programy wymiany igieł i strzykawek oraz leczenie uzależnienia przez programy substytucji. Takie programy mają za zadanie redukcję szkód i kosztów społecznych związanych z epidemią HIV wśród osób przyjmujących dożylnie narkotyki. Zatem ograniczenie negatywnych skutków przyjmowania narkotyków jest oceniane jako ważniejsze niż samo ograniczanie użycia narkotyków. Polityka redukcji szkód nie jest w konflikcie z promocją całkowitej abstynencji od narkotyków, ponieważ trwała abstynencja to najlepszy sposób na ograniczenie szkód związany z przyjmowanie narkotyków.
Programy wymiany sprzętu do wstrzykiwań mogą polegać na nieodpłatnej dystrybucji strzykawek i igieł lub wymianie zużytego sprzętu na nowy. Wymiana sprzętu do wstrzykiwań przyczynia się do zmniejszenia ryzyka udostępniania używanych igieł i strzykawek do ponownego użycia. W licznych badaniach wykazano, że takie programy wymiany sprzętu do wstrzykiwań zmniejszają ryzyko transmisji wirusa HIV. Tworzone są miejsca umożliwiające bezpieczne i sterylne przyjmowanie narkotyków, co ogranicza ponowne używanie skażonych igieł.
W profilaktyce zakażenia HIV u osób uzależnionych od niektórych narkotyków stosuje się leczenie substytucyjne. Największe znaczenie ma leczenie substytucyjne za pomocą metadonu u osób uzależnionych od opiatów. Leczenie substytucyjne zmniejsza ryzyko zakażenia HIV w tej grupie chorych, ponadto zmniejsza ryzyko przedawkowania narkotyku, zmniejsza nielegalne użycie opiatów i przestępczość.
Profilaktyka przenoszenia zakażenia HIV przez transfuzje krwi, przeszczepy tkanek i narządów
W połowie lat 80. wprowadzono przesiewowe badanie dawców w kierunku wirusa HIV. Większość zakażeń za pośrednictwem preparatów krwiopochodnych w krajach rozwijających się przed wprowadzeniem do kwalifikacji dawców krwi badań w kierunku HIV. Zastosowanie testów serologicznych i molekularnych pozwoliło zmarginalizować ryzyko transmisji wirusa HIV poprzez transfuzję preparatów krwiopochodnych. W wytwarzaniu niektórych preparatów krwiopochodnych standardowo stosuje się karencję preparatu oraz techniki inaktywujące wirusa HIV, co dodatkowo zwiększa bezpieczeństwo stosowania tych preparatów. Ryzyko zakażenia poprzez transfuzję krwi jest oceniane na jest 0,14–1,5 przypadków zakażenia na 1 000 000 przetoczeń. Również w przypadku transplantologii dawcy narządów lub tkanek są poddawani badaniom przesiewowym w kierunku HIV.
Profilaktyka przenoszenia zakażenia HIV drogą wertykalną
Ryzyko zakażenia wertykalnego bez profilaktyki jest oceniane na 2255 przypadków na 10 000 przypadków ekspozycji. Zastosowanie odpowiedniej profilaktyki okołoporodowej pozwala znacząco zmniejszyć ryzyko przeniesienia wirusa na dziecko. Kluczowym elementem profilaktyki okołoporodowej zakażeń HIV jest rutynowe badanie w kierunku HIV u kobiet w wieku rozrodczym oraz jako standardowe badanie u kobiet w ciąży. Standardowo badanie w kierunku HIV jest wykonywane w I i III trymestrze ciąży, badanie również jest polecane partnerom ciężarnej. W przypadku ciężarnych, które nie wykonały badania w kierunku HIV, może być wykonywany szybki test w kierunku HIV.
Kobiety z rozpoznanym zakażeniem HIV przed planowaną ciążą powinny otrzymać informacje odnośnie do profilaktyki transmisji zakażenia matka-dziecko. Planowana ciąża może wymagać wdrożenia lub modyfikacji leczenia antyretrowirusowego, które ma celu osiągnięcie maksymalnego zmniejszenia wiremii, szczególnie w okresie okołoporodowym. U par, u których jeden partner nie jest zakażony, w związku z decyzją o zaplanowaniu ciąży konieczna jest profilaktyka zakażenia osoby niezakażonej. W przypadku zakażenia HIV u kobiety w celu profilaktyki niezakażonego partnera stosuje się sztuczne zapłodnienie. Gdy osobą zakażoną jest mężczyzna najbezpieczniejszym rozwiązaniu jest wykorzystanie dawstwa nasienia, a gdy takie rozwiązanie nie jest możliwe, to przed zastosowaniem technik zapłodnienia pozaustrojowego lub sztucznym zapłodnieniem konieczna jest odpowiednia preparatyka, co może zmniejszyć ryzyko ekspozycji na HIV.
Rozpoznanie zakażenia HIV u kobiety w ciąży nie otrzymującej leczenia antyretrowirusowego wymaga wdrożenia takiego leczenia, optymalnie na początku II trymestru ciąży. Późne włączenie leczenia może nie spowodować wystarczającego obniżenia wiremii i wówczas wdraża się leczenie inhibitorem integrazy. U kobiety otrzymującej skuteczne leczenie utrzymuje się je, obecnie nie ma zalecenia bezwzględnej eliminacji ze schematów terapeutycznych efawirenzu. Podobnie leczenie newirapiną może być utrzymane, ale raczej nie włącza się ich do leczenia jeśli nie były stosowane. W trakcie ciąży nie stosuje się stawudyny (d4T), didanozyny (ddI) oraz połączenia trzech nukleozydowych inhibitorów odwrotnej transkryptazy (NRTI).
Ryzyko transmisji HIV ściśle zależy od poziomu wiremii HIV, przyjmuje się, że ryzyko przy wiremii poniżej 1000 kopii/ml wynosi poniżej 1%. Na zwiększenie ryzyka zakażenia wertykalnego wpływa poród przedwczesny, przedwczesne pęknięcie błon płodowych, przedłużony poród czy ekspozycja płodu na krew lub wydzieliny matki. U kobiety otrzymującej HAART i wiremią poniżej 50 kopii/ml (niewykrywalna) zwykle zaleca się poród naturalny. Przy wykrywalnej wiremii (>50 kopii/ml) w 34–38 tygodniu ciąży zaleca się planowe cięcie cesarskie w 38 tygodniu ciąży. W przypadku niewykrywalnej wiremii (poniżej 50 kopii/ml) nie ma potrzeby podawania azydotymidyny (zidowudyna) podczas porodu, jednak gdy wiremia występuje na poziomie powyżej 50 kopii/ml konieczna jest okołoporodowa podaż leku.
Po porodzie noworodek jest dokładnie myty w celu ograniczeniu kontaktu z potencjalnie zakaźnymi wydzielinami matki. Z podobnych powodów konieczne jest odśluzowanie górnych dróg oddechowych noworodka. Niezależnie od nasilenia wiremii u matki u noworodka wdraża się leczenie profilaktyczne. U dzieci matek z niewykrywalną wiremią wdraża się zidowudynę na okres 4 tygodni lub potwierdzenia braku wiremii u noworodka w 3 tygodniu życia. U noworodków matek z oznaczalną niewielką wiremią podaje się zidowudynę przez 4 tygodnie i 3 dawki newirapiny. U noworodków matek z wysoką wiremią podaje się zidowudynę przez 4 tygodnie, lamiwudynę i newirapinę w odpowiednim schemacie łącznie do 14 dni. Innymi opcjami jest podawanie zidowudyny przez 4 tygodnie i newirapiny do 14 dni albo zidowudyny przez 4 tygodnie i 3 dawek newirapiny. U kobiet zakażonym HIV karmienie piersią jest przeciwwskazane, ponieważ niesie ze sobą ryzyko transmisji wirusa.
Profilaktyka przedekspozycyjna (PrEP)
W oparciu o przeprowadzone badania w 2012 WHO zaleciła stosowanie profilaktyki przedekspozycyjnej (pre-exposure prophylaxis, PrEP) jako jeden z elementów ograniczania transmisji HIV. W tym samym roku FDA zatwierdziła pierwszy lek o nazwie Truvada do stosowania w ramach PrEP. W kolejnym dziesięcioleciu na rynku pojawiły się kolejne preparaty – Descovy i Apretude (zastrzyki). Profilaktyka przedekspozycyjna może być stosowana jako ciągła (tabletka zażywana codziennie) lub doraźna (przed i po stosunku). Prawidłowo stosowana charakteryzuje się wysoką skutecznością 50-100% (w zależności od płci partnerów, rodzaju stosunku i stopnia przestrzegania zasad przyjmowania leku).
Rozpoczęcie i stosowanie PrEP wymaga ścisłej kontroli lekarskiej. Na polskim rynku dostępne są preparaty Truvada i Descovy oraz zamienniki.
Profilaktyka poekspozycyjna (PEP)
Działania podjęte po ekspozycji osoby niezakażonej na potencjalnie zakaźny materiał w celu zmniejszenia ryzyka zakażenia HIV nazywane są profilaktyką poekspozycyjną. Ryzyko zakażenia po ekspozycji zależy od rodzaju ekspozycji i materiału zakaźnego. Wyróżnia się ekspozycję zawodową, czyli narażenie na zakażenie materiałem potencjalnie zakaźnym w związku z wykonywaniem pracy, obejmuje to szczególnie zakłucie, skaleczenie, zachlapanie błon śluzowych lub uszkodzonej skóry, ugryzienia, a także ekspozycję niezawodową związaną z kontaktem na materiał zakaźny niezwiązaną z wykonywaniem zawodu, szczególnie ekspozycje seksualne czy dzielenie się sprzętem iniekcyjnym.
Do nieswoistych działań w ramach profilaktyki poekspozycyjnej należy unikanie kontaktu z krwią lub sprzętem zanieczyszczonym krwią, stosowanie indywidualnych środków ochrony osobistej takich jak rękawiczki, maseczki czy okulary ochronne, a także dezynfekcja skażonego płynami ustrojowymi sprzętu medycznego. W przypadku skaleczenia zaleca się umycie rany dużą ilością wody, ewentualnie z użyciem mydła. Nie zaleca się stosowania innych środków odkażających ani hamowania odpływu krwi z rany ani jej wyciskania z rany. Zanieczyszczone śluzówki potencjalnie zakaźnym materiałem kilkukrotnie płucze się wodą lub solą fizjologiczną.
W przypadku ekspozycji przezskórnej, w tym zakłuć i skaleczeń, swoista profilaktyka jest wdrażana, gdy chory od którego pochodzi materiał zakaźny ma rozpoznane zakażenie HIV lub status serologiczny chorego jest nieznany, ale istnieją dodatkowe czynniki zakażenia takie jak zakłucie igłą ze światłem, głębokie zakłucie czy obecności widocznej krwi na narzędziu. W przypadku zachlapania błon śluzowych lub uszkodzonej skóry dużą ilością materiału zakaźnego profilaktyka jest wdrażana w przypadku potwierdzenia dodatniego statusu HIV źródła lub w sytuacji nieznanego statusu serologicznego źródła gdy istnieją dodatkowe czynniki wysokiego ryzyka zakażenia. Zachlapanie błon śluzowych lub uszkodzonej skóry niewielką ilością materiału zakaźnego (kilka kropel) wymaga profilaktyki, tylko w przypadku potwierdzonego dodatniego statusu HIV źródła.
W przypadku ekspozycji pozazawodowej profilaktyka ma zastosowanie wyłącznie w przypadkach incydentalnych. Profilaktyka jest zalecana podczas ekspozycji seksualnej w postaci stosunku analnego lub waginalnego przy potwierdzonym zakażeniu HIV źródła lub nieznanym statusie serologicznym źródła, profilaktykę zaleca się w przypadku stosunku oralnego z wytryskiem przy potwierdzonym zakażeniu HIV źródła. Profilaktyka jest wdrażana u osób używających dożylnych środków odurzających po współdzieleniu sprzętu wstrzykiwań, przy potwierdzonym zakażeniu HIV chorego źródłowego.
Stosowanie leków antyretrowirusowych w ramach profilaktyki poekspozycyjnej zmniejsza ryzyko zakażenia HIV. Zaleca się rozpoczęcie profilaktyki swoistej w ciągu 48 godzin, a wyjątkowo w przypadku ekspozycji o wysokim ryzyku zakażenia do maksymalnie 72 godzin. W profilaktyce poekspozycyjnej stosuje się połączenie 3 leków antyretrowirusowych: połączenie dwóch nukleozydowych/nukleotydowych inhibitorów odwrotnej transkryptazy (tenofowir (TDF)/emtrycytabin (FTC) lub zidowudyna (AZT)/lamiwudyna (3TC) lub lamiwudyna (3TC)/tenofowir (TDF)) oraz inhibitora proteazy (lopinawir (LPV/r) albo inhibitor integrazy (raltegravir (RAL)).
Leczenie antyretrowirusowe
Leczenie zakażenia HIV polega na jednoczesnym skojarzonym zastosowaniu kilku leków antyretrowirusowych. Leczenie ma na celu zmniejszenie replikacji HIV oraz przynajmniej częściową odbudowę układu immunologicznego, a także wydłużenie przeżycia chorych, poprawę jakości ich życia, wzrost liczby limfocytów CD4+ i zmniejszenie częstości chorób związanych z zakażeniem HIV.
Grupy leków antyretrowirusowych
W leczeniu zakażenia HIV stosuje się 5 grup leków antyretrowirusowych: nukleozydowe inhibitory odwrotnej transkryptazy (NRTI), nienukleozydowe inhibitory odwrotnej transkryptazy (NNRTI), inhibitory proteazy (PI), inhibitor fuzji (FI) i inhibitory integrazy (InI).
- Nukleozydowe inhibitory odwrotnej transkryptazy (NRTI)
Nukleozydowe inhibitory odwrotnej transkryptazy (NRTI) są analogami prawidłowych nukleozydów, z powodu braku grupy 3'-OH blokują wydłużanie prowirusowego DNA i przerywają syntezę wirusowego DNA. Do najważniejszych przedstawicieli tej grupy zalicza się abakawir (ABC), emtrycytabina (FTC), lamiwudyna (3TC), tenofowir (TDF), zydowudyna (AZT), alafenamid tenofowiru (TAF).
- Nienukleozydowe inhibitory odwrotnej transkryptazy (NNRTI)
Nienukleozydowe inhibitory odwrotnej transkryptazy (NNRTI) działają poprzez wiązane się w pobliżu miejsca wiązania substratu, co blokuje aktywność enzymu (inhibicja niekompetycyjna). Leki są swoiste dla HIV-1 i nie wykazują aktywności wobec HIV-2 czy ludzkich polimeraz. Do tej grupy leków zalicza się: efawirenz (EFV), etrawiryna (ETV), newirapina (NVP), rilpiwiryna (RPV).
- Inhibitory proteazy (PI)
Inhibitory proteazy blokują postranslacyjną obróbkę nieaktywnego białka wirusowego (Gag-Pol), które musi zostać podzielone przez wirusową proteazę aspartylową proteazę HIV. Inhibitory proteazy wykazując strukturalne podobieństwo do białka wirusowego swoiście blokują proteazę HIV. Zapobiega to tworzenia dojrzałych wirionów i zakażaniu kolejnych komórek. Do inhibitorów proteazy zalicza się indynawir (IDV), nelfinawir (NFV), rytonawir (RTV), sakwinawir (SQV), lopinawir (LPV/r), fosamprenawir (FVP), atazanawir (ATV), typrenawir (TPV) i darunawir (DRV).
- Inhibitory fuzji (wejścia) (FI)
Inhibitory wejścia są grupą leków zapobiegającym fuzji wirusa z komórką docelową. Enfuwirtyd (ENV) poprzez związanie z gp41 zapobiega utworzenie sześciu powiązanych ze sobą spiralnych podjednostek i połączeniu z gp120. Z kolei marawirok (MVC) blokuje interakcję między GP120 a CCR5.
- Inhibitory integrazy (InI)
Integraza jest wirusowym enzymem mającym za zadanie włączenie prowirusowego DNA do materiału genetycznego komórki gospodarzowej. Do leków blokujących aktywność integrazy zalicza się raltegrawir (RAL), elwiregrawir (EVG) i dolutegrawir (DTG).
Wysoce aktywna terapia antyretrowirusowa
Pod koniec lat 80. XX wieku wprowadzono pierwszy skuteczny lek antyretrowirusowy – zydowudynę – jednak leczenie tylko nim szybko prowadziło do wytworzeniu oporności wirusa na ten lek. Postęp w odkrywaniu kolejnych skutecznych grup leków antyretrowirusowych w połowie lat 90. pozwolił na leczenie za pomocą kombinacji kilku leków antyretrowisowych. Połączenie trzech leków antyretrowirusowych o synergistycznej aktywności antyretrowirusowej jest nazywane wysoce aktywną terapią antyretrowirusową (HAART). Ta wielolekowa terapia znacząco poprawiła skuteczność leczenia, zdecydowanie obniżając umieralność powodowaną chorobą. HAART pozwoliła przekształcić chorobę nieuchronnie prowadzącą do śmierci w chorobę przewlekłą i umożliwiło długie przeżycie chorych. Ponadto leczenie, redukując wiremię, obniża ryzyko transmisji wirusa.
Leczenie ma na celu zmniejszenie replikacji HIV oraz przynajmniej częściową odbudowę układu immunologicznego, a także wydłużenie przeżycia chorych, poprawę jakości ich życia, wzrost liczby limfocytów CD4+ i zmniejszenie częstości chorób związanych z zakażeniem HIV.
Kluczowe jest nieprzerwane przyjmowanie leków w zaleconych dawkach przyjmowanych o określonych porach, nieprzestrzeganie schematu leczenia sprzyja selekcji mutantów wirusa opornych na leki. Nie zaleca się czasowego planowego przerywania leczenia antyretrowirusowego i nie stosuje się krótkotrwałych ani długotrwałych przerw od leczenia, ponieważ sprzyjają one wzrostowi wiremii wirusa, pogorszeniu funkcji układu immunologicznego, progresji klinicznej oraz rozwojowi lekooporności.
Rozpoczynanie leczenia antyretrowirusowego
Leczenie antyretrowirusowe powinno być włączone u wszystkich zakażonych wirusem HIV niezależnie od stanu klinicznego oraz liczby limfocytów CD4+. Wczesne rozpoczynanie leczenia antyretrowirusowego niezależnie od liczby limfocytów CD4+ prowadzi do poprawy przeżycia i zmniejszenia ryzyka niektórych chorób niedefiniujących AIDS, szczególnie sercowo-naczyniowych, nerek, wątroby, neurodegeneracyjnych i nowotworowych. Również mniejsze jest ryzyko progresji choroby, obserwuje się lepszą odbudowę układu immunologicznego i zmniejsza ryzyko transmisji HIV.
U chorych bezobjawowych odroczenie leczenia jest możliwe w przypadku braku gotowości chorego do leczenia, ponieważ brak odpowiedniej współpracy chorego może skutkować zwiększonym ryzykiem generowania oporności na leki. U chorych z gruźlicą leczenie zaczyna się najpierw od wdrożenia 8 tygodniowego leczenia przeciwprątkowego, a następnie wdrożenia leczenia antyretrowirusowego. U chorych z liczbą limfocytów CD4+ <50 komórek/μl leczenie antyretrowirusowe zaczyna się wcześniej, w ciągu 2 tygodni od rozpoczęcia leczenia przeciwprątkowego.
Pierwsza linia leczenia
Podczas wyboru leków składających się na pierwszą linię leczenia uwzględnia się poziom wiremii HIV, liczbę limfocytów CD4+, wyjściową oporność wirusa na leki, choroby współistniejące, koinfekcję HBV lub HCV, stosowane inne leki, ciążę lub planowanie ciąży oraz styl życia chorego. Pozwala to na odpowiednie dobranie leków o określonym profilu toksyczności i dawkowaniu, co sprzyja ich prawidłowemu stosowaniu. Ze względu na uproszczenie dawkowania i leczenia w miarę możliwości wybierane są preparaty złożone składające się z kilku leków antyretrowirusowych. W leczeniu preferowanymi schematami są połączenia dwóch nukleozydowych inhibitorów odwrotnej transkryptazy (NRTI) z nienukleozydowym inhibitorem odwrotnej transkryptazy (NNRTI) lub w połączeniu z inhibitorem proteazy (PI) wzmocnionym rytonawirem (RTV) lub w połączeniu z inhibitorem integrazy (InI). Według zaleceń WHO preferuje się połączenie tenofowiru z lamiwudyną (TDF + 3TC) z efawirenzem (EFV) albo połączenie tenofowiru z emtrycytabiną (TDF + FTC) z efawirenzem (EFV). Jeśli powyższy schemat jest przeciwwskazany lub nie jest dostępny, to stosuje się połączenie zydowudyny, lamiwudyny i efawirenzu (AZT + 3TC + EFV), zydowudyny, lamiwudyny i newirapiny (AZT + 3TC + NVP), tenofowiru, lamiwudyny lub emtrycytabiny i newirapiny (TDF + 3TC lub FTC + NVP).
Zmiana leczenia antyretrowirusowego
- Niepowodzenie leczenia antyretrowirusowego
Nadrzędnym celem leczenia jest supresja replikacji wirusa HIV poniżej 50 kopii/ml po 6 miesiącach leczenia. W przypadku stwierdzenia wiremii powyżej 50 kopii/ml po 6 miesiącach leczenia lub w dwóch kolejnych oznaczenia po wcześniejszym osiągnięciu pełnej supresji wirusologicznej. Przyczyną może być lekooporność wirusa, wysoka wyjściowa wiremia, wcześniejsze rozpoznanie AIDS, niska wyjściowa liczba limfocytów CD4+, interakcje lekowe, działania niepożądane, choroby współistniejące, stosowanie środków psychoaktywnych i brak stosowania się przez chorego do zaleceń.
Zaleca się, w miarę dostępności badania, wykonanie badania lekooporności wirusa na leki antyretrowirusowe. Po uzyskaniu wyniku badania dalsze leczenie jest prowadzone o profil oporności. Nowy schemat powinien zawierać przynajmniej dwa aktywne leki, a optymalnie trzy aktywne leki. Jeśli nie ma możliwości leczenia za pomocą przynajmniej dwóch leków konieczne może być odłożenie zmiany leczenia. Jednak może być to niemożliwe u chorych z liczbą limfocytów CD4+ <100 komórek/μl lub znacznym pogorszeniem stanu klinicznego.
- Działania niepożądane
W przypadku wystąpienia uciążliwych działań niepożądanych może być konieczne odstawienie podejrzanego o ich spowodowanie leku, a czasem nawet całego zestawu leków.
Działania niepożądane leczenie antyretrowirusowego
Choć leczenie znacząco wydłuża życie chorych, to jednak jest związane z istotnym ryzykiem wystąpienia działań niepożądanych.
- Nadwrażliwość
Jednym z najczęściej występujących działań niepożądanych stosowania leków antyretrowirusowych dotyczą reakcji nadwrażliwości. U około 5% leczonych abakawirem z antygenami zgodności tkankowej HLA B*5701 w początkowym okresie stosowania może występować potencjalnie zagrażająca życiu reakcja nadwrażliwości z gorączką, bólami brzucha, nudnościami i wymiotami. Leku nie stosuje się u osób z rozpoznanym genotypem HLA B*5701. U 20% chorych podczas leczenia newirapiną i delawirdyną pojawia się wysypka na tułowiu i ramionach.
- Zaburzenia ze strony przewodu pokarmowego
Stosunkowo często na początku leczenia zydowudyną pojawiają się nudności i wymioty, a podczas stosowania inhibitorów proteazy, zydowudyny i didanozyny pojawia się biegunka. Didanozyna może być powodem ostrego zapalenia trzustki.
- Hepatotoksyczność
Cechy uszkodzenia wątroby są częstym następstwem leczenia. W wyniku zaburzenia fosforylacji oksydacyjnej kwasów tłuszczowych dochodzi do stłuszczenia wątroby. W przebiegu leczenia nienukleozydowymi inhibitorami odwrotnej transkryptazy może dojść do uszkodzenia wątroby w przebiegu reakcji nadwrażliwości. Z kolei u chorych zakażonych HBV czy HCV po włączeniu leczenia antyretrowirusowego może dojść do zespołu rekonstrukcji immunologicznej i ciężkiego uszkodzenia wątroby.
- Zaburzenia metaboliczne
U 15% leczonych pojawia się podwyższone stężenie mleczanów. Wyjątkowo dochodzi do rozwoju kwasicy mleczanowej, która potencjalnie jest stanem grożącym zgonem. Kwasica mleczanowa jest związana głównie ze stosowaniem NRTI, szczególnie z d4T, ddI i AZT.
U chorych leczonych inhibitorami proteazy może rozwinąć się insulinooporność i w konsekwencji cukrzyca. Nukleozydowe inhibitory odwrotnej transkryptazy, nienukleozydowe inhibitory transkryptazy i inhibitory proteazy sprzyjają powstawaniu hiperlipidemii. Zaburzenia lipidowe i insulinooporność stanowią element zespołu lipodystrofii i wpływają na zwiększenie ryzyka rozwoju chorób sercowo-naczyniowych oraz zapalenia trzustki.
- Zespół lipodystrofii
Zespół lipodystrofii jest zespołem zaburzeń metabolicznych prowadzących do zaburzeń gospodarki lipidowej i węglowodanowej oraz redystrybucji tkanki tłuszczowej. Na zespół składa się zanik tkanki tłuszczowej (lipoatrofia) w obrębie kończyn, pośladków, policzków, okolicy skroniowej i oczodołów, a także nasilenie nagromadzenia tkanki tłuszczowej (lipohipertrofia) w zakresie trzewi, karku i sutków. Prowadzi to do zmiany sylwetki i wyglądu chorego. W ramach zespołu może występować hiperlipidemia i insulinooporność.
- Powikłania hematologiczne
Podczas leczenia zydowudyną, indinawirem, abakawirem i tenofowirem może pojawić się leukopenia. Niedokrwistość może być następstwem leczenia zydowudyną, powikłanie zwykle pojawia się w ciągu pierwszych 3 miesięcy leczenia, ale może pojawić się znacznie później po wielu miesięcy leczenia.
- Działanie nefrotoksyczne
Tenofowir może wykazywać działanie nefrotoksyczne.
- Powikłania sercowo-naczyniowe
U osób leczonych lekami antyretrowirusowymi obserwuje się zwiększone ryzyko sercowo-naczyniowe, co jest związane z insulinoopornością i hiperlipidemią.
Szczególne sytuacje kliniczne
Koinfekcja wirusami HBV i HCV
Ze względu na podobne drogi szerzenia wirusa HIV i wirusów hepatotropowych u chorych zakażonych HIV znacznie częściej obserwuje się jednoczesne zakażenie (koinfekcja) wirusami hepatropowymi: wirusem zapalenia wątroby typu C (HCV) oraz zakażeniem wirusem zapalenia wątroby typu B (HBV).
Koinfekcję HIV i HBV w zależności od regionu świata obserwuje się u od 5 do 20% zakażonych HIV. Koinfekcja HCV i HIV dotyczy, w zależności od regionu i dominującej drogi transmisji wirusa, około 10–15% chorych, przy czym u chorych na HIV przyjmujących dożylnie narkotyki częstość koinfekcji HCV wynosi aż 50–90%.
Wirusy HBV i HCV mogą prowadzić w różnym odsetku odpowiednio do przewlekłego zapalenia wątroby typu B i C, a ostatecznie do marskości wątroby i raka wątrobowokomórkowego. W związku z wprowadzeniem leczenia antyretrowirusowego, które pozwoliło w znacznym stopniu kontrolować zakażenia oportunistyczne i związaną z nimi śmiertelność, marskość wątroby związana z zakażeniem wirusami hepatropowymi stała się wiodącą przyczyną zgonów zakażonych HIV i odpowiada za około 9% z nich. Koinfekcja HIV i HBV zwiększa ryzyko i przyspiesza progresje przewlekłego zapalenia wątroby typu B do marskości, a także ryzyko raka wątrobowokomórkowego i zgonu. Zakażenia HBV nie wpływa na ryzyko progresji zakażenia HIV i odsetek odpowiedzi na HAART. Z kolei wpływ zakażenia HCV na przebieg zakażenia HIV jest niejasny. Prawdopodobnie koinfekcja HIV i HCV zwiększa ryzyko wystąpienia chorób sercowo-naczyniowych oraz schyłkowej niewydolności nerek.
Analogi nukleozydowe wykazują jednoczesną aktywność wobec wirusów HIV oraz HBV. Leczenie przewlekłego wirusowego zapalenia wątroby typu B jest prowadzone równocześnie z leczeniem antyretrowirusowym, ponieważ brak zahamowania replikacji HIV podczas leczenia zakażenia HBV może doprowadzić do wyselekcjonowania szczepów opornych. Zwykle stosuje się tenofowir w połączeniu z lamiwudyną lub emtrycytabiną, pozostałe leki leczenia antyretrowirusowego są dobierane na ogólnych zasadach.
W przypadku przewlekłego wirusowego zapalenia wątroby typu C leczenie HCV jest stosowane u wszystkich chorych, którzy mogą odnieść z niego korzyść. Ze względu na interakcje i toksyczność leczenie HCV i HIV jest prowadzone w jednym ośrodku. Dobór schematów bezinterferonowych stosowanych w leczeniu HCV uwzględnia genotyp wirusa oraz funkcję wątroby. Z kolei dobór schematu leczenia antyretrowirusowego musi uwzględniać interakcje lekowe.
Zakażenie HIV u dzieci
Co roku rozpoznaje się około 240 000 nowych przypadków zakażenia wirusem HIV u dzieci i młodzieży poniżej 15 roku życia, szacuje się, że na świecie żyje 3,2 miliona dzieci zakażonych HIV. Zdecydowana większość zakażonych HIV dzieci żyje w Afryce Subsaharyjskiej. U trzech czwartych dzieci drogę zakażenia stanowi okołoporodowa transmisja wirusa z matki na dziecko. Drugą grupę zakażonych stanowią zakażenia nabyte w wieku nastoletnim poprzez ryzykowne kontakty seksualne. Zakażenie HIV u dzieci przebiega znacznie szybciej niż u osób dorosłych. Obserwuje się znacznie wyższe poziomy wiremii HIV w porównaniu do osób dorosłych. Szybko dochodzi do progresji do AIDS. U nieleczonych niezależnie od ocenionego stopnia niedoboru odporności pojawiają się ciężkie zakażenia oportunistyczne. Dochodzi do zaburzenia rozwoju centralnego układu nerwowego, innych zaburzeń rozwojowych i niedoborów wzrostu.
U dzieci powyżej 18 miesiąca życia w rozpoznaniu zakażenia HIV stosowane są testy immunoenzymatyczne wykrywające przeciwciała anty-HIV oraz testy potwierdzenia, przede wszystkim western blot na podobnych zasadach jak u osób dorosłych. Do 18 miesiąca życia u dziecka obecne są odmatczyne przeciwciała anty-HIV, których obecność nie świadczy o zakażeniu wirusem HIV u dziecka. W diagnostyce u dzieci poniżej 18. miesiąca życia konieczne jest oznaczenie obecności materiału genetycznego wirusa HIV. U wszystkich dzieci matek zakażonych HIV w 14–21 dniu życia wykonuje się badanie PCR wykrywające HIV RNA. Kolejne oznaczenie przeprowadza się po 30 dniu życia pomiędzy 1. a 2. miesiącem życia, ale jeśli noworodek otrzymywał profilaktykę 2-3 lekową badanie wykonuje się po 2–4 tygodniach od zakończenia tej profilaktyki. Trzecie badanie jest wykonywane około 4–6. miesiąca życia. Wstępne wykluczenie zakażenia HIV jest możliwe po dwukrotnym ujemnym wyniku HIV RNA z 2-3 tygodnia i 1-2 miesiąca życia. Dodatni wynik wymaga potwierdzenia kolejnym testem PCR HIV RNA. Po 6 miesiącu życia oznacza się również przeciwciała anty-HIV i dwukrotnie ujemny wynik anty-HIV również umożliwia wykluczenie zakażenia. Jednak ze względu na możliwość nieutworzenia przeciwciał anty-HIV u dzieci możliwa jest sytuacja potwierdzania obecności wiremii HIV bez obecnych przeciwciał anty-HIV.
Leczenie antyretrowirusowe jest dostosowywane do wieku chorego dziecka, farmakokinetyki i danych dotyczących bezpieczeństwa leków wchodzących w skład terapii w tej grupie wiekowej. Leczenie jest prowadzone w ośrodkach specjalistycznych. U dzieci powyżej 2 roku życia leczenie zaleca się u wszystkich dzieci, a do bezwzględnych wskazań należy wiremia powyżej 100 000 kopii/ml, obecność objawów zakażenia (kategoria przynajmniej B według CDC) lub umiarkowany niedobór odporności (kategoria 2 według CDC). U dzieci poniżej 2 roku życia leczenie wdraża się niezależnie od objawów klinicznych i wartości wiremii.
Rokowanie
U większości nieleczonych chorych zakażenie HIV w ciągu 10 lat ulega progresji do AIDS i chory umiera w ciągu kolejnych 2 lat. Leczenie antyretrowirusowe znacząco wydłuża przeżycie chorych. Większość chorych otrzymujących HAART przeżywa ponad 10 lat. W dużej metaanalizie na ponad 290 000 chorych otrzymujących leczenie antyretrowirusowe u 87% stwierdzono 2-letnie, 86% 4-letnie, 78% 8-letnie, 78% 10-letnie i 61% 12-letnie przeżycie do wystąpienia progresji do AIDS. Z kolei u chorych otrzymujących leczenie antyretrowirusowe rozwijających AIDS opisano prawdopodobieństwo przeżycia 87% 2-letniego, 86% 4-letniego, 78% 6-letniego, 78% 8-letniego i 61% 10-letniego.
Uwagi
Bibliografia
- Janusz Cianciara, Jacek Juszczyk: Choroby zakaźne i pasożytnicze. Lublin: CZELEJ, 2007. ISBN 978-83-60608-34-0.
- Andrzej Szczeklik, Piotr Gajewski: Interna Szczeklika 2014. Kraków: Medycyna Praktyczna, 2014. ISBN 978-83-7430-405-4.
- John E. Bennett, Raphael Dolin, Martin J. Blaser: Mandell, Douglas, and Bennett's Principles and Practice of Infectious Diseases. Elsevier Health Sciences, 2014. ISBN 978-0-323-26373-3.
- S. Kartikeyan, R. N. Kartikeyan, R. P. Tiwari, P. S. Bisen: HIV and AIDS: Basic Elements and Priorities. Springer Science & Business Media, 2007. ISBN 978-1-4020-5789-2.
- Andrzej Gładysz: Zakażenia HIV/AIDS poradnik dla lekarzy praktyków. Continuo, 2007. ISBN 978-83-89629-78-4.
- Gary W. Procop, Bobbi Pritt: Pathology of Infectious Diseases: A Volume in the Series: Foundations in Diagnostic Pathology. Elsevier Health Sciences, 2014. ISBN 978-1-4557-5384-0.
- Andrzej Horban, Regina Podlasin, Grażyna Cholewińska, Alicja Wiercińska-Drapało, Brygida Knysz: Zasady opieki nad osobami zakażonymi HIV. Zalecenia polskiego towarzystwa naukowego AIDS 2016. 2016. ISBN 978-83-925140-9-1.
- Paul Volberding: Global HIV/AIDS Medicine. Elsevier Health Sciences, 2008. ISBN 978-1-4160-2882-6.
- Waldemar Halota, Jacek Juszczak: HIV/AIDS. Podręcznik dla lekarzy i studentów. Termedia, 2006.
- Zdzisław Dziubek: Choroby zakaźne i pasożytnicze. PZWL, 2010. ISBN 978-83-200-3768-5.
- Michael G. Katze, Marcus J. Korth, G. Lynn Law, Neal Nathanson: Viral Pathogenesis: From Basics to Systems Biology. Academic Press, 2015. ISBN 978-0-12-801174-4.
- Ernst Mutschler, Gerd Geisslinger, Heyo K. Kroemer, Peter Ruth, Monika Schäfer-Korting: Farmakologia i toksykologia. Wrocław: MedPharm Polska, 2010. ISBN 978-83-60466-81-0.
- John C. Hall, Brian John Hall, Clay J. Cockerell: HIV/AIDS in the Post-HAART Era: Manifestations, Treatment, Epidemiology. PMPH-USA, 2011. ISBN 978-1-60795-206-0.
- Meg Doherty, Rachel Beanland, Andrew Ball: Consolidated guidelines on The use of Antiretroviral drugs For treating and Preventing hiv infection 2016 Recommendations for a Public health approach. 2016.